题目内容
4.如图是实验室制备物质、探究物质性质的常用装置,请回答:
(1)连接装置A、E可用来制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)除去CO中少量的C02,最好将气体通过装置D;
(3)连接装置B、C可用来验证CO的还原性,CO通过装置B时可以看到红色粉末变成黑色装置C中出现的白色浑浊,那么,装置B中发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据反应装置可知反应物和反应条件,据此写出化学反应式;
(2)比较氢氧化钙和氢氧化钠的溶解性,再在了解浓溶液的吸收性更强的基础上作出选择;
(3)根据题意和观察图示可知是一氧化碳还原氧化铜的实验,据此写出CO通过装置B时可以看到的现象;根据化学方程式的书写方法分析解答.
解答 解:(1)连接装置A、E可用来制取氧气,装置A应与E的c端连接,因为氧气的密度比空气的大;如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)氢氧化钙微溶于水,氢氧化钠易溶于水,相同条件下,等质量的水溶解的氢氧化钠多,配制浓溶液吸收二氧化碳效果好,最好的装置选D;
(3)连接装置B、C可用来验证CO的还原性,CO通过装置B时可以看到红色粉末变成黑色;反应发生后会看到装置C中出现白色浑浊,说明有二氧化碳生成,装置B中发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
故答案为:
(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)D;
(3)红色粉末变为黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
15.下列操作不正确的是( )
| A. | 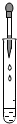 滴加液体 | B. |  检验氧气 | C. | 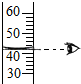 读取液体体积 | D. |  取用固体 |
12.对下列事实的解释正确的是( )
| A. | 点燃所有可燃性气体前都应先验纯--防止气体不纯点燃时爆炸 | |
| B. | 空气能被压缩--分子的体积变小 | |
| C. | 浓硫酸、氢氧化钠溶液露置在空气中质量都增加--都发生了变质 | |
| D. | 铝的抗腐蚀性比铁强--铁比铝更容易与氧气反应 |
9.对下列化学反应的基本类型判断正确的是( )
| A. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O分解反应 | |
| B. | CaCO3+CO2+H2O═Ca(HCO3)2合成反应 | |
| C. | 2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑复分解反应 | |
| D. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C交换反应 |
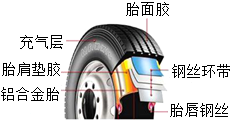 汽车轮胎是汽车的重要部件.市场上存在个别轮胎原料掺假问题:以返炼胶代替原片胶,严重影响轮胎的质量,给采用该轮胎的汽车带来了安全隐患.如图是汽车轮胎示意图,请回答下列问题:
汽车轮胎是汽车的重要部件.市场上存在个别轮胎原料掺假问题:以返炼胶代替原片胶,严重影响轮胎的质量,给采用该轮胎的汽车带来了安全隐患.如图是汽车轮胎示意图,请回答下列问题: 如图为部分元素的离子结构示意图.其中属于阳离子的是②(填序号);选择其中的两种元素组成AB2型化合物,其化学式是MgCl2.
如图为部分元素的离子结构示意图.其中属于阳离子的是②(填序号);选择其中的两种元素组成AB2型化合物,其化学式是MgCl2.