题目内容
16.各组物质能在pH=1.5的溶液中大量共存,且都成无色溶液的是( )| A. | NaCl BaCl2 Na2SO4 | B. | Na2SO4 HCl KCl | ||
| C. | CuSO4 NaCl NaNO3 | D. | Na2CO3 NaCl Na2SO4 |
分析 pH为1.5的水溶液显酸性,水溶液中含有大量的H+;根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存;本题还要注意能得到无色溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为1.5的水溶液显酸性,水溶液中含有大量的H+:
A、BaCl2 和 Na2SO4在溶液中能相互交换成分生成硫酸钡沉淀和氯化钠,不能共存,故选项错误;
B、H+和Na2SO4 HCl KCl三者之间不能结合成沉淀、气体或水,能大量共存,且不存在有色离子,故选项正确;
C、H+和CuSO4 NaCl NaNO3三者之间不能结合成沉淀、气体或水,能大量共存,但CuSO4 溶液显蓝色,故选项错误;
D、H+和Na2CO3 中的碳酸根离子结合生成水和二氧化碳,不能大量共存,故选项错误;
故选B.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意特定离子的颜色.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.除去下列物质中的杂质,所选用的试剂和操作方法都正确的是( )
| 编号 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | 氮气 | 氧气 | 铜 | 通过灼热的铜网 |
| B | 氯化亚铁溶液 | 氯化锌 | 足量铁 | 过滤 |
| C | 氯化钾 | 二氧化锰 | 水 | 溶解、过滤、洗涤、干燥 |
| D | 稀硫酸 | 稀盐酸 | 适量硝酸银溶液 | 过滤 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
7.海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库.
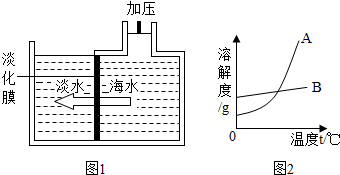
(1)地球上可供人类使用的淡水仅占地球上总水量的0.3%,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义,海水淡化的方法很多,如图1是采用膜法淡化海水的示意图,当对淡化膜右侧的海水加压时,在其左侧可得到淡水,其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过,请回答下列问题:
①在混合物分离的常见物理方法中,过滤操作与膜法淡化海水的原理相似.
②对淡化膜右侧的海水加压后,右侧剩余溶液中溶质的质量分数会增大(填“增大”、“减小”、“不变”之一)
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,KNO3和NaCl在不同温度时的溶解度如下表所示,请回答下列问题:
①依据上表数据,可绘制出KNO3和NaCl的溶解度曲线如图2所示,图中能表示KNO3溶解度曲线的是A(填“A”或“B”);
②在20℃时,向盛有200g水的烧杯中加入100gKNO3,充分溶解,可得到该温度时KNO3的饱和(填“饱和”、“不饱和”之一)溶液,若烧杯内物质缓慢升温至60℃,在该温度下,最后所得溶液中溶质与溶液的质量之比为1:3(填最简整数比).

(1)地球上可供人类使用的淡水仅占地球上总水量的0.3%,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义,海水淡化的方法很多,如图1是采用膜法淡化海水的示意图,当对淡化膜右侧的海水加压时,在其左侧可得到淡水,其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过,请回答下列问题:
①在混合物分离的常见物理方法中,过滤操作与膜法淡化海水的原理相似.
②对淡化膜右侧的海水加压后,右侧剩余溶液中溶质的质量分数会增大(填“增大”、“减小”、“不变”之一)
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,KNO3和NaCl在不同温度时的溶解度如下表所示,请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |
②在20℃时,向盛有200g水的烧杯中加入100gKNO3,充分溶解,可得到该温度时KNO3的饱和(填“饱和”、“不饱和”之一)溶液,若烧杯内物质缓慢升温至60℃,在该温度下,最后所得溶液中溶质与溶液的质量之比为1:3(填最简整数比).