题目内容
将H2、CO、CO2、N2组成的混合气体,依次通过下面盛有足量试剂的实验装置,实验完毕可收集到纯净干燥的N2.
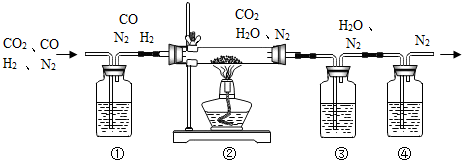
图①~④中可供选择的试剂由:a、浓硫酸;b、稀硫酸;c、氢氧化钠溶液;d、澄清石灰水;e、铜粉;f、氧化铜粉
请根据下表中所述的实验现象或作用填空.

图①~④中可供选择的试剂由:a、浓硫酸;b、稀硫酸;c、氢氧化钠溶液;d、澄清石灰水;e、铜粉;f、氧化铜粉
请根据下表中所述的实验现象或作用填空.
| 装置中的实验现象或作用 | 选择一种试剂(填编号) | 化学方程式 |
| 瓶①的溶液澄清透明 | 瓶① | |
| 装置②中黑色粉末变红色 | 瓶② | |
| 瓶③溶液由澄清变混浊 | 瓶③ | |
| 瓶④溶液起干燥气体作用 | 瓶④ |
考点:常见气体的检验与除杂方法,书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:根据题意:混合气体通过装置后得到纯净干燥的氮气,并据物质的性质和实验现象分析解答:氢氧化钠能更好的吸收二氧化碳,一氧化碳、氢气具有还原性,可与氧化铜反应,二氧化碳可使澄清的石灰水变浑浊,浓硫酸具有吸水性,常作干燥剂.
解答:解:根据题意:混合气体通过装置后得到纯净干燥的氮气,并结合图示气体通过①后二氧化碳被吸收,氢氧化钠可充分吸收二氧化碳,因为氢氧化钠极易溶于水,发生反应的方程式是:CO2+2NaOH=Na2CO3+H2O;
通过②后氢气和一氧化碳被除去,说明试管中放置的是能与二者反应的氧化铜粉末,氢气和氧化铜加热生成铜和水,方程式是H2+CuO
Cu+H2O,一氧化碳和氧化铜加热生成铜和二氧化碳,方程式是CO+CuO
Cu+CO2;
气体通过③后溶液由澄清变浑浊,说明瓶中装的溶液是澄清的石灰水,与二氧化碳反应生成不溶于水的碳酸钙沉淀和水,方程式是CO2+Ca(OH)2═CaCO3↓+H2O;
瓶④溶液起干燥气体作用,说明瓶内装的是浓硫酸,因为浓硫酸具有吸水性,可用来干燥气体;
故答案为:
通过②后氢气和一氧化碳被除去,说明试管中放置的是能与二者反应的氧化铜粉末,氢气和氧化铜加热生成铜和水,方程式是H2+CuO
| ||
| ||
气体通过③后溶液由澄清变浑浊,说明瓶中装的溶液是澄清的石灰水,与二氧化碳反应生成不溶于水的碳酸钙沉淀和水,方程式是CO2+Ca(OH)2═CaCO3↓+H2O;
瓶④溶液起干燥气体作用,说明瓶内装的是浓硫酸,因为浓硫酸具有吸水性,可用来干燥气体;
故答案为:
| 装置中的实验现象或作用 | 选择一种试剂(填编号) | 化学方程式 | ||||||||
| 瓶①的溶液澄清透明 | 瓶①c | CO2+2NaOH=Na2CO3+H2O | ||||||||
| 装置②中黑色粉末变红色 | 瓶②f | H2+CuO
| ||||||||
| 瓶③溶液由澄清变混浊 | 瓶③d | CO2+Ca(OH)2═CaCO3↓+H2O | ||||||||
| 瓶④溶液起干燥气体作用 | 瓶④a | 无 |
点评:此题是一道综合题,解题的重点是实验中各装置的作用的掌握及对气体性质的了解,是一道能训练学生思维的综合题.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列说法正确的是( )
| A、工业上常采用分离液态空气法制氧气,该原理是利用氮气和氧气的密度不同进行分离 |
| B、实验是制取气体的原料必须是纯净物 |
| C、氧气的化学性质比较活泼,属于可燃物 |
| D、空气质量报告中所列的空气质量级别越小,空气质量越好 |
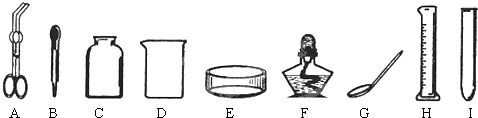
 经过一年的初中化学学习,我们认识了许多化学实验仪器,也知道了不少实验操作的要求.
经过一年的初中化学学习,我们认识了许多化学实验仪器,也知道了不少实验操作的要求.