题目内容
15.化学是一门以实验为基础的科学,请结合图1回答问题: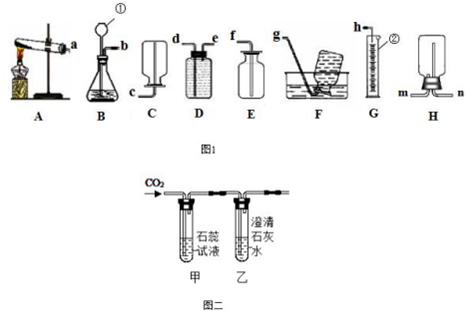
(1)写出仪器①的名称:①长颈漏斗.
(2)小杜同学准备用高锰酸钾制取并收集一瓶纯净的氧气,选择了A(选装置字母)
作为发生装置,他选择的依据是反应物状态和反应条件,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若还想利用 H 装置收集一瓶干燥的氧气,则氧气应该从m端进入(填“m 或 n”).
(3)小彭同学设计了如图2所示装置验证二氧化碳的性质,当通入二氧化碳一段时间后,用化学方程式解释甲装置中颜色变化的原因H2O+CO2═H2CO3.小张同学将变红的甲装置取下,放在酒精灯上充分加热,她看到的现象是溶液由红色变为紫色.乙装置中澄清石灰水变浑浊,反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
(4)小聂同学在实验室用锌粒和稀硫酸常温制取氢气,并测定生成氢气的体积,他将从 A~G
中选择最佳的装置进行组合,整套装置的导管口连接顺序是b→e→d→h(填接口序号).
分析 (1)根据实验室常用仪器解答;
(2)依据高锰酸钾制取氧气的反应原理书写表达式,并据反应物的状态和反应条件选择发生装置,氧气不易溶于水,用排水法可收集较纯净的氧气;
(3)根据二氧化碳与水反应生成碳酸解答;根据二氧化碳与石灰水反应生成碳酸钙沉淀的性质解答;
(4)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;量筒可以用来量取一定量的液体.
解答 解:
(1)根据实验室常用仪器可知:①长颈漏斗;
(2)高锰酸钾在加热下分解为锰酸钾、二氧化锰和氧气,因为反应物为固体,反应条件为加热,所以发生装置选A,氧气不易溶于水,用排水法可收集较纯净的氧气,方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;氧气的密度比空气的大,若还想利用 H 装置收集一瓶干燥的氧气,则氧气应该从m端进入;
(3)二氧化碳与水反应生成碳酸,紫色石蕊试液遇酸变红,F中发生反应的化学方程式为:CO2+H2O=H2CO3;将变红的甲装置取下,放在酒精灯上充分加热,她看到的现象是溶液由红色变为紫色,碳酸不稳定,加热分解为二氧化碳和水;
二氧化碳与石灰水反应生成碳酸钙沉淀,故澄清的石灰水中通入二氧化碳的实验现象是:澄清的石灰水变浑浊;反应方程式是:Ca(OH)2+CO2=CaCO3↓+H2O;
(4)氢气的密度比水的小,小聂同学在实验室用锌粒和稀硫酸常温制取氢气,并测定生成氢气的体积,他将从 A~G中选择最佳的装置进行组合,整套装置的导管口连接顺序是b→e→d→h.
答案:
(1)①长颈漏斗;
(2)A; 反应物状态和反应条件;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)H2O+CO2═H2CO3;溶液由红色变为紫色; Ca(OH)2+CO2═CaCO3↓+H2O;
(4)e→d→h.
点评 本题难度不大,掌握高锰酸钾制取氧气的反应原理、氧气的检验方法,发生和收集装置的选取方法并会应用即可顺利解答.

 名校课堂系列答案
名校课堂系列答案| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
(1)该花汁可以(填“可以”或“不可以”)作酸碱指示剂.
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的肥皂水.
(3)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式NaHCO3+HCl═NaCl+H2O+CO2↑.
(4)石灰水暴露于空气中易变质,写出变质反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O.
①酸 ②碱 ③盐 ④氧化物.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
| A. | 铝合金门窗 | B. | 玻璃 | C. | 陶瓷地板 | D. | 木制桌凳 |