题目内容
将10克氢气和氧气的混合气体点燃并充分反应,发现还剩余1克氢气,则原混合气体中氢气和氧气的质量比为( )
| A、1:9 | B、1:8 |
| C、1:4 | D、2:1 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据充分反应后还剩余1克氢气,由质量守恒定律可知生成水的质量:10g-1g=9g,利用化学反应方程式可知,可求出参加反应氢气和氧气的质量来分析解答.
解答:解:充分反应后还剩余1克氢气,由质量守恒定律可知生成水的质量:10g-1g=9g.
设参加反应反应的氢气和氧气的质量分别为x、y;
2H2+O2
2H2O
4 32 36
x y 9g
=
x=1g
=
y=8g
则原混合气体中氢气和氧气的质量比=(1g+1g):8g=1:4.
故选:C.
设参加反应反应的氢气和氧气的质量分别为x、y;
2H2+O2
| ||
4 32 36
x y 9g
| 4 |
| x |
| 36 |
| 9g |
x=1g
| 32 |
| y |
| 36 |
| 9g |
y=8g
则原混合气体中氢气和氧气的质量比=(1g+1g):8g=1:4.
故选:C.
点评:在解此类题时,首先根据题中的条件列出关系式,解出题中需要的量,然后结合题意在进一步解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学符号既表示一种元素,又表示一个原子,同时还表示一种物质的是( )
| A、H2 | B、O |
| C、NO | D、C |
核内质子数相同,核外电子数不同的两种粒子,它们可能是( )
| A、两种不同元素的原子 |
| B、同种元素的原子和离子 |
| C、同种元素的两种离子 |
| D、不同种元素的原子和离子 |
下列物质属于无机化合物的是( )
| A、矿泉水 | B、锌 |
| C、高锰酸钾 | D、蔗糖 |
乙醇俗称酒精,其分子式是C2H5OH,有关该物质的下列说法错误的是( )
| A、该物质是有机物,常用溶剂,属可再生能源 |
| B、该物质燃烧后的产物不会影响PM2.5值 |
| C、一个分子中含有9个原子 |
| D、分子中碳、氢、氧三种元素的质量比为2:6:1 |
以下叙述中正确的是 ( )
| A、需要加热才能发生的变化是化学变化 |
| B、不需要加热就能发生的变化是物理变化 |
| C、伴随有发光发热现象的变化一定是化学变化 |
| D、物质燃烧时发生化学变化 |
 试用你学过的化学知识解释下列问题或现象.
试用你学过的化学知识解释下列问题或现象.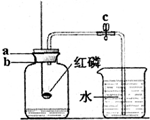 如图是空气中氧气含量测定的实验装置,请回答下列问题:
如图是空气中氧气含量测定的实验装置,请回答下列问题: