题目内容
12. 农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇分子的结构模型如图所示,则下列叙述正确的是( )
农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇分子的结构模型如图所示,则下列叙述正确的是( )| A. | 乙醇是氧化物 | B. | 一个乙醇分子共有26个质子 | ||
| C. | 乙醇中碳、氧元素的质量比为3:4 | D. | 乙醇中氧元素的质量分数最大 |
分析 A.根据氧化物的概念来分析;B.根据分子结构和原子结构来分析;C.根据化合物中元素质量比的计算方法来分析;D.根据化合物中元素质量分数大小的比较方法来分析.
解答 解:根据乙醇的分子结构模型可知,1个乙醇的分子由2个碳原子、6个氢原子和1个氧原子所构成,乙醇的化学式可表示为C2H6O.
A.由乙醇的化学式可知,它含有三种元素,不符合氧化物是由两种元素组成的特征,故错误;
B.1个乙醇分子是由两个碳原子、六个氢原子和一个氧原子构成的,一个碳原子中含有6个质子、1个氢原子含有1个质子、1个氧原子中含有8个质子,所以一个乙醇分子中含有26个质子,故正确;
C.乙醇中碳、氧元素的质量比为(12×2):(16×1)=3:2,故错误;
D.由乙醇C2H6O中碳、氢、氧元素的质量比=(12×2):(1×6):16=12:3:8,可判断乙醇中碳元素的质量分数最大,而非氧元素的质量分数最大,故错误.
故选B.
点评 本题考查化学式的意义以及化学式的简单计算,综合性较强,进一步考查原子的构成,属于简单的信息给予题型,通过结构式获得所需的信息.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
3.根据如图判断,下列说法正确的是( )
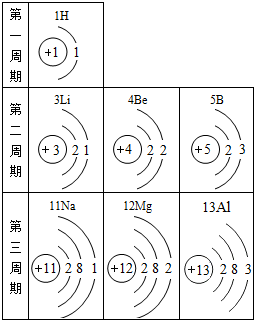

| A. | 铝的相对原子质量是13 | |
| B. | 钠离子核外有三个电子层 | |
| C. | 在化学变化中镁元素的原子容易得到2个电子形成镁离子 | |
| D. | 第二、三周期元素的原子从左边至右最外层电子数逐渐增多 |
20.下列变化中属于物理变化的是( )
| A. | 鞭炮爆炸 | B. | 食物腐败 | C. | 冰雪融化 | D. | 钢铁生锈 |
1.反应MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑常用于实验室制取氯气,在反应的反应物和生成物中,不存在的物质种类是( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氯化物 |
2.空气中含量最多的元素是( )
| A. | H | B. | O | C. | C | D. | N |
