题目内容
某硝酸铵样品,经分析其中氮元素的质量分数为37%,则样品中可能含的杂质是( )
| A、NH4HCO3 |
| B、(NH4)2SO4 |
| C、NH4Cl |
| D、CO(NH2)2 |
考点:元素的质量分数计算
专题:化学式的计算
分析:先求出硝酸铵中氮元素的质量分数然后与37%比较,然后利用平均值法则解决并判断.
解答:解:NH4NO3氮元素的质量分数为
×100%=35%<37%,故混入的化肥含氮量大于37%.
A、碳铵的含氮量为:
×100%=17.1%,小于37%,故此答案错误.
B、(NH4)2SO4的含氮量为:
×100%=21%,小于37%,故此选项错误.
C、NH4Cl的含氮量为:
×100%=26.19%,小于37%,故此答案错误.
D、尿素的含氮量为:
×100%=47%,大于37%,故此答案正确.
故选:D.
| 2×14 |
| 1×14+4+16×3 |
A、碳铵的含氮量为:
| 14 |
| 14+5+12+16×3 |
B、(NH4)2SO4的含氮量为:
| 14×2 |
| (14+4)×2+32+16×4 |
C、NH4Cl的含氮量为:
| 14 |
| 14+4+35.5 |
D、尿素的含氮量为:
| 14×2 |
| 12+16+(14+2)×2 |
故选:D.
点评:此题是结合平均值法则进行的化学式计算题,是对学生进行常规计算及方法的训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列气体混合物,遇明火可能发生爆炸的是( )
| A、H2 CO2 |
| B、CO O2 |
| C、H2 CO |
| D、CO N2 |
下列物质间的转化,不能通过一步反应实现的是( )
| A、CO2→CO |
| B、CO2→CaCO3 |
| C、CO→H2CO3 |
| D、Fe2O3→Fe |
将铁片放入下列溶液中,过一会儿后取出称量,其质量增加的是( )
| A、稀硫酸 | B、稀盐酸 |
| C、硫酸铜溶液 | D、硫酸亚铁溶液 |
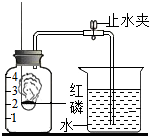 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: