题目内容
18.某实验小组取一定量的氯酸钾和二氧化锰混合后加热制取氧气,充分反应后实验剩余固体25.4g,将固体加水充分溶解后,再向溶液中滴加足量的硝酸银溶液,反应后过滤、洗涤得到固体39.2g,计算原混合物中氯酸钾的含量为( )| A. | 50% | B. | 70% | C. | 80% | D. | 98% |
分析 根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,充分反应后实验剩余固体25.4g,是氯化钾和二氧化锰混合物的质量;将固体加水充分溶解后,再向溶液中滴加足量的硝酸银溶液,氯化钾能与硝酸银溶液反应生成氯化银白色沉淀和硝酸钾,反应后过滤、洗涤得到固体39.2g,得到的固体比25.4g增加了39.2g-25.4g=13.8g,由固体差量法计算出原混合物中氯酸钾的质量、二氧化锰的质量,进而计算出原混合物中氯酸钾的含量.
解答 解:设原混合物中氯酸钾的质量为x,生成氯化钾的质量为y,
KCl+AgNO3═KNO3+AgCl↓ 固体质量差量=143.5-75.5=69
由2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑、KCl+AgNO3═KNO3+AgCl↓,可得:
则KClO3~KCl~AgCl
122.5 74.5 固体质量差量=69
x y 39.2g-25.4g=13.8g
$\frac{122.5}{69}=\frac{x}{13.8g}$ x=24.5g
$\frac{74.5}{69}=\frac{y}{13.8g}$ y=14.9g
则原混合物中二氧化锰的质量为25.4g-14.9g=10.5g.
原混合物中氯酸钾的含量为$\frac{24.5g}{24.5g+10.5g}$×100%=70%.
故选:B.
点评 本题难度不大,掌握利用化学方程式的计算方法、明确反应的原理与之间的关系并能灵活运用是正确解答本题的关键.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
8.下列说法错误的是( )
| A. | 电解水时有氢气和氧气产生,所以水是由氢气和氧气组成的 | |
| B. | 化学变化的实质是分子破坏,原子重新组合 | |
| C. | 在化学变化中,元素种类不变,原子种类和数目不变 | |
| D. | 由不同种分子构成的物质一定是混合物 |
9.将N2、CO、CO2混合气体通过足量石灰水,再通过炽热的氧化铜后,剩余气体是( )
| A. | CO2 | B. | CO和N2 | C. | N2 | D. | CO2和N2 |
6.以下实验,对现象的描述不正确是( )
| A. | 木炭在氧气中剧烈燃烧,发出白光,放出热量,反应后倒入澄清石灰水变浑浊 | |
| B. | 硫粉在氧气中燃烧更旺,火焰呈明亮的蓝紫色,生成有刺激性气味的气体,放出热量 | |
| C. | 红磷在氧气中燃烧更旺,发出白光,产生大量的白烟,放出热量 | |
| D. | 镁条在空气中剧烈燃烧,发出耀眼的白光,放出热量,生成氧化镁 |
 用如图所示的装置探究空气中氧气的含量.实验过程如下:
用如图所示的装置探究空气中氧气的含量.实验过程如下: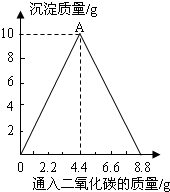 已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的石灰水中通入CO2,产生沉淀的量与通入CO2气体的量的关系如图所示,回答下列问题:
已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的石灰水中通入CO2,产生沉淀的量与通入CO2气体的量的关系如图所示,回答下列问题:
 从2014年1月至今,在几个月的时间里,全国范围内媒体曝光的自来水异味事件已达10起,日前发生的兰州水污染事件,更加引起了从们对于水的质量关注.水源地污染的情况非常严重,让人触目惊心.因此珍惜水、爱护水源是我们每个公民应尽的义务和责任.
从2014年1月至今,在几个月的时间里,全国范围内媒体曝光的自来水异味事件已达10起,日前发生的兰州水污染事件,更加引起了从们对于水的质量关注.水源地污染的情况非常严重,让人触目惊心.因此珍惜水、爱护水源是我们每个公民应尽的义务和责任.