题目内容
7.食盐是一种重要的化工原料.请回答下列问题.(1)如图1是实验室除去粗盐中泥沙等难溶性杂质的实验步骤.
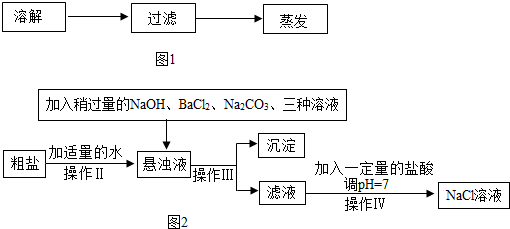
①过滤所用的玻璃仪器有:烧杯、漏斗和玻璃棒,该仪器的作用是引流.
②在蒸发过程中,待蒸发皿中出现较多量固体时,停止加热,利用余热将滤液蒸干.应使用坩埚钳(填仪器名称)取下热的蒸发皿,放于石棉网上.
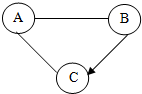
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如图2.
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是BaCl2+Na2CO3=BaCO3↓+2NaCl(用化学方程式表示).
②加入的氢氧化钠溶液要过量的目的是将粗盐中含有的氯化镁完全除去.
③操作Ⅲ的名称是过滤,通过操作Ⅲ所得滤液中的溶质有NaCl、NaOH、Na2CO3(用化学式表示).
分析 (1)根据过滤和蒸发的操作及注意事项分析回答;
(2)①根据碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠进行分析;
②根据氢氧化钠能与氯化镁反应分析;
③根据实验的过程和加入的各种除杂试剂进行分析.
解答 解:(1)①过滤所用的玻璃仪器有:烧杯、漏斗和玻璃棒,该仪器的作用是引流.
②在蒸发过程中,待蒸发皿中出现较多量固体时,停止加热,利用余热将滤液蒸干.应使用坩埚钳取下热的蒸发皿,放于石棉网上.
(2))①碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;
②氢氧化钠能与氯化镁反应生成了氢氧化镁沉淀和氯化钠,所以加入的氢氧化钠溶液要过量的目的是:将粗盐中含有的氯化镁完全除去;
③操作Ⅲ的名称是过滤,通过分析可知,加入的碳酸钠、氢氧化钠都是过量的,还有生成的氯化钠,所以通过操作Ⅲ所得滤液中的溶质有:NaOH、NaCl、Na2CO3.
故答为:(1)①玻璃棒,引流.②蒸发皿中出现较多量固体.坩埚钳.(2)①BaCl2+Na2CO3=BaCO3↓+2NaCl;②将粗盐中含有的氯化镁完全除去.③过滤.NaCl、NaOH、Na2CO3.
点评 海水的综合利用是初中化学中较为重要的内容之一,与之相关的实验操作,药品的选用,化学方程式的书写等都是经常考查的内容,同学们一定要对此内容了然于心.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
18.下列各组物质的名称、俗称、化学式表示同一种物质的是( )
| A. | 氢氧化钠、纯碱、Na2CO3 | B. | 氯化银、食盐、NaCl | ||
| C. | 硫酸铜晶体、胆矾、CuSO4•5H2O | D. | 碳酸钙、生石灰、Ca(OH)2 |
2.能一次性鉴别NaOH、Ca(OH)2、稀盐酸三种溶液的试剂是( )
| A. | 氯化铜溶液 | B. | 紫色石蕊试液 | C. | 酚酞试剂 | D. | 碳酸钠溶液 |
16.下列四个实验方案设计不合理的是( )
| A.认识物质俗名 | B.注意实验安全 |
| ①固体二氧化碳--干冰 ②氢氧化钙--熟石灰 ③氢氧化钠--纯碱 | ①点燃可燃性气体前一定要验纯 ②鉴别化学药品时可以品尝 ③危险实验配戴防护眼镜 |
| C.合理利用资源 | D.健康生活方式 |
| ①随意大量使用塑料袋 ②过量使用农药、化肥提高农业产量 ③钢铁表面刷上油漆,防止钢铁生锈 | ①平衡膳食,不偏食挑食 ②不购买食用过期食品 ③不过量饮用碳酸饮料 |
| A. | A | B. | B | C. | C | D. | D |
 A、B、C为初中化学常见物质,既他们之间有如下图所示关系(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).
A、B、C为初中化学常见物质,既他们之间有如下图所示关系(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).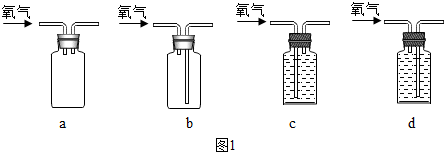
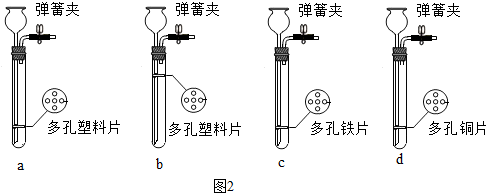
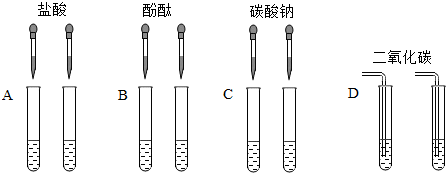
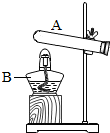 绘制实验设计图是填写实验报告常用的一项重要技能.如图是某同学正在绘制的实验室用氯酸钾和二氧化锰制取氧气的装置图.
绘制实验设计图是填写实验报告常用的一项重要技能.如图是某同学正在绘制的实验室用氯酸钾和二氧化锰制取氧气的装置图.