题目内容
14、下列曲线错误的是( )
分析:A、氢氧化钠溶液显碱性,可以与稀盐酸反应生成氯化钠和水,据此进行分析判断;
B、由向水中加浓硫酸的过程中溶质的质量分数的变化趋势进行分析判断;
C、稀硝酸加水稀释酸性会减弱,pH会增大,但不会大于7;
D、反应在在密闭容器中,结合质量守恒定律进行分析判断.
B、由向水中加浓硫酸的过程中溶质的质量分数的变化趋势进行分析判断;
C、稀硝酸加水稀释酸性会减弱,pH会增大,但不会大于7;
D、反应在在密闭容器中,结合质量守恒定律进行分析判断.
解答:解:A、盐酸与氢氧化钠反应生成氯化钠和水,当加入的盐酸与氢氧化钠反应完全后,生成氯化钠的质量不再增加,故图象正确;
B、向水中加入浓硫酸,溶质的质量分数逐渐增大,故图象正确;
C、稀硝酸显酸性,加水酸性会减弱,pH会增大,但不会大于7而变成碱性溶液,故图象错误.
D、反应在密闭容器中进行,所以反应前后物质的总质量不变,故图象正确.
故选C.
B、向水中加入浓硫酸,溶质的质量分数逐渐增大,故图象正确;
C、稀硝酸显酸性,加水酸性会减弱,pH会增大,但不会大于7而变成碱性溶液,故图象错误.
D、反应在密闭容器中进行,所以反应前后物质的总质量不变,故图象正确.
故选C.
点评:解答此类题的关键是要抓住三个点(起点、转折点、终点)、一个意义(图象的纵横坐标表示的意义)及对图象涉及的化学反应原理进行分析判断.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
如图为甲、乙两种固体物质(不含结晶水)在水中的溶解度曲线.下列说法错误的是( )
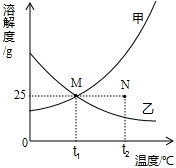

| A、N点可表示t2℃时甲物质的不饱和溶液 | B、tl℃时,甲物质饱和溶液的溶质质量分数是20% | C、将等质量的甲、乙饱和溶液分别从t2℃降温至tl℃,所得溶液的溶质质量分数大小关系:W(甲)=W(乙) | D、当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲 |
甲、乙两种固体物质的溶解度曲线如图所示,下列叙述错误的是( )
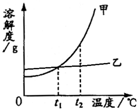

| A、t2℃时,甲的溶解度比乙的大 | B、升高温度可将甲的饱和溶液变成不饱和溶液 | C、提纯甲、乙(少)混合物中的甲,采用蒸发溶剂结晶 | D、t1℃时,甲和乙溶液中溶质质量分数一定相等 |
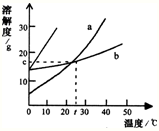 a、b两种固体物质的溶解度曲线如图,下列说法错误的是( )
a、b两种固体物质的溶解度曲线如图,下列说法错误的是( ) (2008?清远)近几年木糖醇作为新型的甜味剂正在悄悄地替蔗糖进入生活,在某温度下其溶解度分别为:30℃时70g,50℃时84个g,60℃时90g,如图表示的是木糖醇等固体的溶解度曲线.根据曲线判断下列说法错误的是( )
(2008?清远)近几年木糖醇作为新型的甜味剂正在悄悄地替蔗糖进入生活,在某温度下其溶解度分别为:30℃时70g,50℃时84个g,60℃时90g,如图表示的是木糖醇等固体的溶解度曲线.根据曲线判断下列说法错误的是( )