题目内容
取氯酸钾和二氧化锰的混合物26g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质址为16 .4g ,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10%的氯化钾溶液(假设溶液无损失)。计算:
(1)生成氧气的质量。
(2)二氧化锰的质量。
( 3)氯化钾溶液中水的质量。
(1)生成氧气的质量为26g-16.4g=9.6g;
(2)设:原混合物中氯酸钾的质量为x,生成氯化钾的质量为y
245 149 96
X y 9.6g

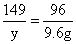
X=24.5g y=14.9g
所以二氧化锰的质量为26g—24.5g=1.5g
(3)根据题意易知氯酸钾已全部分解,生成氯化钾的质量为14.9g
所以氯化钾溶液质量为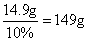
氯化钾溶液中水的质量为149g—14.9g=134.1g
答:(1)生成氧气质量为9.6g
(2)二氧化锰的质量为1.5g
(3)氯化钾溶液中水的质量为134.1g

已知化学反应Al2O3+2NaOH=2R+H2O,推断R的化学式是( )
|
| A. | Na2O | B. | Al(OH)3 | C. | NaAlO2 | D. | NaAlO |
在下面关系图中,A、B、C、D是初中化学中常见的单质,甲、乙分别是酒精燃烧时一定会产生的两种物质,丁是常用建筑材料的主要成分,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,J是赤铁矿的主要成分。
 |
(1)写出化学式:甲是 ,G是 ;
(2)写出H与J反应的化学方程式: ;
(3)J溶解于稀盐酸中,溶液呈黄色,反应完全后,再向溶液中加入纯净的D的粉末,溶液逐渐变成浅绿色,写出有关变化的化学方程式:
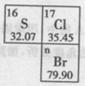

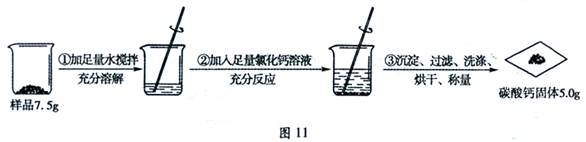

 (1)鸡蛋含有的营养素主要为 。
(1)鸡蛋含有的营养素主要为 。