题目内容
15.小光同学在2016年合肥中考理科实验操作“氢氧化钠溶液的性质”实验中,向盛有硫酸铜溶液的试管中滴加氢氧化钠溶液,发现刚开始时无明显现象,继续滴加后才出现蓝色絮状沉淀.小光思考这是什么原因?与同学继续进行了如下实验探究:[作出假设]假设:CuSO4溶液显酸性.
[实验过程]
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学 | 向一洁净试管中加入2mLCuSO4溶液,向其中滴加石蕊试液 | 现象石蕊试液变红 | 假设成立 |
| 乙同学 | 向一洁净试管中加入2mLCuSO4溶液,向其中加入一定量铁粉 | 现象:①先生成气泡,后蓝色逐渐消失,溶液变成绿色 ②首先反应的化学方程式:Fe+H2SO4=FeSO4+H2↑ |
分析 根据硫酸铜溶液可以和氢氧化钠溶液反应生成蓝色沉淀,可以据此写出该反应的化学方程式.
解答 解:
甲同学:向一洁净试管中加入2mLCuSO4溶液,向其中滴加石蕊试液,溶液变红,说明溶液显酸性.
乙同学:向一洁净试管中加入2mLCuSO4溶液,加入一定量铁粉,开始有气泡产生,说明是铁和酸反应生成氢气,然后铁和硫酸铜反应生成硫酸亚铁和铜.Fe+H2SO4=FeSO4+H2↑.
通过实验可知:盐溶液不一定是中性的.
故答案为:
| 验操作 | 实验现象 | 实验结论 | |
| 甲同学 | 向一洁净试管中加入2mLCuSO4溶液,向其中滴加 石蕊试液 | 现象石蕊试液变红 | 假设成立 |
| 乙同学 | 向一洁净试管中加入2mLCuSO4溶液,向其中加入一定量铁粉 | 现象:①:先生成气泡,后蓝色逐渐消失,溶液变成绿色 ; ②首先反应的化学方程式:Fe+H2SO4=FeSO4+H2↑ |
点评 想解答好这类题目,首先,要理解和熟记碱的化学性质、反应现象和化学方程式,以及与之相关的知识.然后,根据所给的实验,结合所学的相关知识和技能,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
5.日常生活中发生的下列变化,都属于化学变化的是( )
| A. | 汽油燃烧、石油分馏出汽油、柴油 | |
| B. | 湿衣服晾干、利用膜法从海水中获得淡水 | |
| C. | 菜刀生锈、工业上从空气中分离出氧气 | |
| D. | 将铁矿石炼成生铁、植物光合作用 |
6.屠呦呦是第一位获得诺贝尔科学奖项的中国本土科学家.1972年,屠哟哟和她的同事在青蒿中提取到了一种分子式为C15H22O5的无色结晶体,一种熔点为156℃〜157℃的活性成份,他们将这种无色的结晶体物质命名为青蒿素.青蒿素为一具有“高 效、速效、低毒,优点的新结构类型抗疟药,对各型疟疾特别是抗恶性疟疾有特效.关 于青蒿素下列说法正确的是( )
| A. | 属于氧化物 | B. | 由碳元素、氢元素、氧元素组成 | ||
| C. | 282g青蒿素中含有86g碳元素 | D. | 一个青蒿素分子中含有5个氧分子 |
3.下列各组中的两种物质,在只用水作试剂的情况下,不能进行鉴别的是( )
| A. | CaCO3、Na2CO3 | B. | NaCl、Na2SO4 | C. | FeCl3、NaCl | D. | NH4NO3、NaCl |
10.某农民家有一种失去标签的化肥,该化肥可能是碳酸氢铵、氯化铵或硫酸钾中的一种.某化学兴趣小组为帮他确定该化肥的成分,进行了下列实验.
【反思与评价】
(1)小凯认为,不进行上述实验也能确定此化肥的种类,他采用的方法是直接闻气味,若有氨味,则为碳酸氢铵.
(2)结合实验步骤一,请你写出使用氨态氮肥的一点注意事项铵态氮肥不能与碱性物质混合施用.
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取样,加入少量的熟石灰,混合研磨 | 嗅到氨味 | 该化肥一定不是硫酸钾 |
| 步骤二:另取少许样品,加入少量的盐酸 | 有大量气泡产生 | 该化肥是碳酸氢铵.发生的化学方程式为NH4HCO3+HCl═NH4Cl+H2O+CO2↑ |
(1)小凯认为,不进行上述实验也能确定此化肥的种类,他采用的方法是直接闻气味,若有氨味,则为碳酸氢铵.
(2)结合实验步骤一,请你写出使用氨态氮肥的一点注意事项铵态氮肥不能与碱性物质混合施用.
20.实验室四瓶失去标签的无色溶液分别为氯化钠溶液、稀盐酸、氢氧化钠溶液和稀硫酸.以下说法正确的是( )
| A. | 打开试剂瓶塞就可以判断出稀盐酸------瓶口有“白雾” | |
| B. | 观察试剂瓶的瓶塞可以判断出氢氧化钠溶液-------是胶塞 | |
| C. | 打开试剂瓶塞尝味道可以判断出氯化钠溶液------有咸味 | |
| D. | 将pH试纸伸入试剂瓶中可以判断出稀硫酸-------pH小于7 |
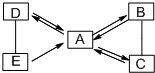 如图所示,A、B、C、D、E均为初中化学所涉及的常见物质,它们存在如下图的转化关系.C是空气的重要组成成分,B是人体内直接供能物质.B、C、D属于不同类别的物质.(“→”表示物质之间的转化关系,“-”表示物质之间可以发生化学反应)
如图所示,A、B、C、D、E均为初中化学所涉及的常见物质,它们存在如下图的转化关系.C是空气的重要组成成分,B是人体内直接供能物质.B、C、D属于不同类别的物质.(“→”表示物质之间的转化关系,“-”表示物质之间可以发生化学反应)