题目内容
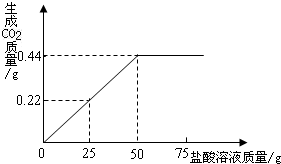 某同学在对3g混有碳酸钠的氯化钠固体样品进行分析时,发现滴加盐酸的质量与生成二氧化碳气体的质量恰好符合右图所示的质量关系.若反应中产生的二氧化碳气体全部逸出无损失且质量测定准确,试计算:当碳酸钠恰好完全反应时,所得溶液中溶质的质量分数.(计算结果精确到0.01%)
某同学在对3g混有碳酸钠的氯化钠固体样品进行分析时,发现滴加盐酸的质量与生成二氧化碳气体的质量恰好符合右图所示的质量关系.若反应中产生的二氧化碳气体全部逸出无损失且质量测定准确,试计算:当碳酸钠恰好完全反应时,所得溶液中溶质的质量分数.(计算结果精确到0.01%)
分析:反应后所得溶液为氯化钠溶液,其中溶质氯化钠由原样品中氯化钠和反应生成的氯化钠两部分组成,因此需要分别计算出两部分氯化钠的质量;而反应后所得溶液质量可利用质量守恒定律进行计算.
解答:解:分析图中反应的质量关系知:至碳酸钠恰好完全反应时,所需稀盐酸的质量为50g,反应中共得到0.44g二氧化碳气体
设混合物中碳酸钠的质量为x,反应后新生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 117 44
x y 0.44g
则:
=
,x=1.06g
=
,y=1.17g
故至碳酸钠恰好反应时,所得溶液的溶质质量分数为:
×100%=5.92%
答:当碳酸钠恰好完全反应时,所得溶液的溶质质量分数为5.92%
设混合物中碳酸钠的质量为x,反应后新生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 117 44
x y 0.44g
则:
| 106 |
| x |
| 44 |
| 0.44g |
| 117 |
| y |
| 44 |
| 0.44g |
故至碳酸钠恰好反应时,所得溶液的溶质质量分数为:
| 3g-1.06g+1.17g |
| 3g+50g-0.44g |
答:当碳酸钠恰好完全反应时,所得溶液的溶质质量分数为5.92%
点评:根据化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算中反应中其它物质的质量.

练习册系列答案
相关题目
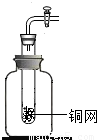
 (2008?义乌市)如如图所示为某同学在实验室利用底部有破洞的试管和广口瓶组装成的制取二氧化碳的发生装置.实验时广口瓶中应盛有
(2008?义乌市)如如图所示为某同学在实验室利用底部有破洞的试管和广口瓶组装成的制取二氧化碳的发生装置.实验时广口瓶中应盛有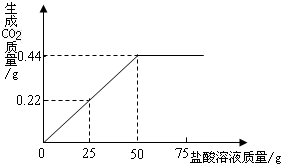 某同学在对3g混有碳酸钠的氯化钠固体样品进行分析时,发现滴加盐酸的质量与生成二氧化碳气体的质量恰好符合右图所示的质量关系.若反应中产生的二氧化碳气体全部逸出无损失且质量测定准确,试计算:当碳酸钠恰好完全反应时,所得溶液中溶质的质量分数.(计算结果精确到0.01%)
某同学在对3g混有碳酸钠的氯化钠固体样品进行分析时,发现滴加盐酸的质量与生成二氧化碳气体的质量恰好符合右图所示的质量关系.若反应中产生的二氧化碳气体全部逸出无损失且质量测定准确,试计算:当碳酸钠恰好完全反应时,所得溶液中溶质的质量分数.(计算结果精确到0.01%)