题目内容
9.造纸是我国古代四大发明之一,它有效地推动了人类文明的发展.(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的空气污染,秸秆的主要成份是纤维素[(C6H10O5)n],纤维素中C、H、O三种元素的质量比为36:5:40(用最简整数比表示).
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放.
①用pH试纸检测废水呈碱性的简单方法是用洁净干燥的玻璃棒蘸取处理后的废水,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH.
②若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可以处理的废水质量是多少?(写出计算过程)
分析 根据物质的化学式可以计算组成元素的质量比;
利用pH试纸可以测定溶液的酸碱度;
稀硫酸和氢氧化钠反应生成硫酸钠和水,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)纤维素中C、H、O三种元素的质量比为:(12×6):(1×10):(16×5)=36:5:40.
故填:36:5:40.
(2)①用pH试纸检测废水呈碱性的简单方法是:用洁净干燥的玻璃棒蘸取处理后的废水,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH,从而可知氢氧化钠溶液显碱性.
故填:用洁净干燥的玻璃棒蘸取处理后的废水,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH.
②设处理废水的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
x×1.6% 9.8t×20%
$\frac{80}{x×1.6%}$=$\frac{98}{9.8t×20%}$,
x=100t,
答:可以处理氢氧化钠溶液100t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14. “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O═2Mg(OH)2.电池发生的反应属于( )
“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O═2Mg(OH)2.电池发生的反应属于( )
 “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O═2Mg(OH)2.电池发生的反应属于( )
“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O═2Mg(OH)2.电池发生的反应属于( )| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
1. 春暖花开,某校九年级同学外出春游.请回答下列问题:
春暖花开,某校九年级同学外出春游.请回答下列问题:
出发前,小乐购买某品牌自热米饭.
①某品牌自热米饭的食品成分包括:米饭、鸡肉、油菜等,其中富含糖类的是米饭.
②菜肴包的包装材料 是铝箔.金属铅可以压制成铝箔,说明其具有良好的延展性.
③饭盒底部有用塑料膜密封的生石灰,使用时需将膜撕掉,并倒入水,这时会发生反应,该反应是化学能转化为热能.
到达景区,同学们陶醉了!
④景区繁花似锦,鸟语花香,从分子的角度解释“花香四溢”的原因分子不断运动.
⑤玫瑰花香中含有香茅醇、橙花醇和丁香酚等物质,其中丁香油酚(C16H12O2)属于有机物(选“有机物”或“无机物”)
春游回来,小海打算到化学实验室研究从景区带回的一块鹅卵石,想用实验证明鹅卵石中是否含有碳酸盐?请你参与此项研究.
 春暖花开,某校九年级同学外出春游.请回答下列问题:
春暖花开,某校九年级同学外出春游.请回答下列问题:出发前,小乐购买某品牌自热米饭.
①某品牌自热米饭的食品成分包括:米饭、鸡肉、油菜等,其中富含糖类的是米饭.
②菜肴包的包装材料 是铝箔.金属铅可以压制成铝箔,说明其具有良好的延展性.
③饭盒底部有用塑料膜密封的生石灰,使用时需将膜撕掉,并倒入水,这时会发生反应,该反应是化学能转化为热能.
到达景区,同学们陶醉了!
④景区繁花似锦,鸟语花香,从分子的角度解释“花香四溢”的原因分子不断运动.
⑤玫瑰花香中含有香茅醇、橙花醇和丁香酚等物质,其中丁香油酚(C16H12O2)属于有机物(选“有机物”或“无机物”)
春游回来,小海打算到化学实验室研究从景区带回的一块鹅卵石,想用实验证明鹅卵石中是否含有碳酸盐?请你参与此项研究.
| 实验步骤 | 实验现象 | 实验结论 |
| ⑥将石块敲碎,取少量于试管中,加入适量的稀盐酸. | 无明显现象 | 鹅卵石中不含碳酸盐 |
18.下列关于分子、原子离子的认识正确的是( )
| A. | 它们构成的物质都不显电性 | |
| B. | 它们在化学变化中都不能再分 | |
| C. | 分子在不停地运动,原子和离子不会运动 | |
| D. | 分子的质量较大,原子和离子的质量较小 |
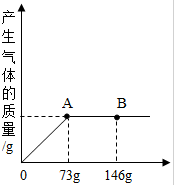 一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:
一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:



