题目内容
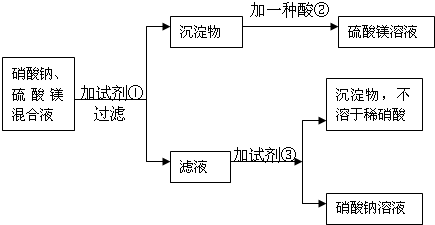
我国某些盐湖出产的天然碱中含有的杂质为氯化钠及少量泥沙.某校初三学生为了测定该天然碱中碳酸钠的质量分数,提出了两个测定方案,具体过程如图:
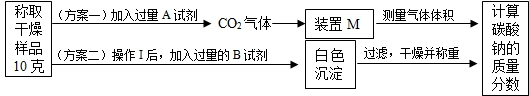
(1)A试剂的化学式是 ,A试剂须“过量”的原因是 .
(2)方案二中“操作1”应是 操作.

(1)A试剂的化学式是
(2)方案二中“操作1”应是
考点:盐的化学性质,过滤的原理、方法及其应用
专题:常见的盐 化学肥料
分析:盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应;天然碱中含有的杂质为氯化钠及少量泥沙,方案一是加入过量的稀盐酸,过量的目的是让碳酸钠充分反应,通过测量二氧化碳的质量,求碳酸钠的质量分数;方案二中先把不溶性杂质泥沙除去,应该先进行过滤,因此“操作1”应是过滤;再加入过量的氯化钙溶液,通过称量沉淀的质量来计算碳酸钠的质量分数.
解答:解:(1)方案一是加入过量的稀盐酸,过量的目的是让碳酸钠充分反应,通过测量二氧化碳的质量,求碳酸钠的质量分数;故答案为:HCl;让碳酸钠充分反应;
(2)方案二中先把不溶性杂质泥沙除去,应该先进行过滤,因此“操作1”应是过滤;再加入过量的氯化钙溶液,通过称量沉淀的质量来计算碳酸钠的质量分数;故答案为:过滤;
(2)方案二中先把不溶性杂质泥沙除去,应该先进行过滤,因此“操作1”应是过滤;再加入过量的氯化钙溶液,通过称量沉淀的质量来计算碳酸钠的质量分数;故答案为:过滤;
点评:本考点属于盐的性质中实验方法和过程的探究,根据物质的溶解性和除杂质的条件,要认真分析,把握实验设计的每一个步骤中的实验目的即可.本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
相关题目
下列变化中,既有物理变化又有化学变化的是( )
| A、用金刚石切割玻璃 |
| B、石灰石被粉碎 |
| C、蜡烛燃烧 |
| D、铜线被弯曲 |
下列变化中,属于化学变化的是( )
| A、酒精挥发 |
| B、工业上用空气制取氧气 |
| C、冰受热熔化成水 |
| D、蓝色硫酸铜晶体受热变成白色粉末 |
根据质量守恒定律判断:在化学反应X+3O2
2CO2+3H2O中,X的化学式为( )
| ||
| A、CH3OH |
| B、CH3COOH |
| C、C2H6OH |
| D、CH4 |
人们在生产、生活中,为了防止事故发生,常采用一些安全措施.下列措施安全的是( )
| A、到溶洞探险打火把照明 |
| B、到矿井埯挖煤来禁烟火 |
| C、清理沼气池前先进行火把试验 |
| D、用燃着的木条检查液化石油气是否泄漏 |
下列各组物质中,属于纯净物的一组是( )
| A、蒸馏水、液态氧、液态氢 |
| B、稀硫酸、稀盐酸、氢氧化钠溶液 |
| C、新鲜空气、纯净食盐水、清洁矿泉水 |
| D、汽水、浓硫酸、大理石 |
下列有关物质的应用中,具有重大伤害事故隐患的是( )
| A、用活性炭作冰箱除臭剂 |
| B、用二氧化碳灭火 |
| C、用干冰进行人工降雨 |
| D、庆典活动时使用大量氢气球 |