题目内容
14.某种硫的氧化物,其中硫元素和氧元素的质量比为2:3,则该氧化物中硫原子和氧原子的个数比为( )| A. | 2:3 | B. | 3:2 | C. | 1:3 | D. | 3:1 |
分析 根据题意,在硫的一种氧化物中,硫元素与氧元素的质量比为2:3,由两种原子的相对原子量,计算出该化合物中硫元素与氧元素的原子个数之比即可.
解答 解:在硫的一种氧化物中,硫元素和氧元素的质量比为2:3,硫原子和氧原子的相对原子质量分别为32、16,则可设硫的氧化物化学式为SxOy;则$\frac{32x}{16y}=\frac{2}{3}$,则1个该硫的氧化物中硫原子和氧原子的个数比为x:y=1:3.
故选:C.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
20.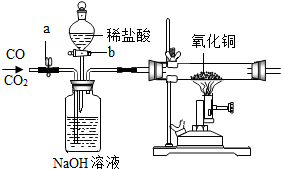 现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )
现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )
 现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )
现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )| A. | 只收集到CO气体 | B. | 只收集到CO2气体 | ||
| C. | 先收集到CO气体,后收集到CO2气体 | D. | 先收集到CO2气体,后收集到CO气体 |
1.厨房里发生的化学变化中,属于物理变化的是( )
| A. |  煤气燃烧 | B. |  面包发霉 | C. |  榨取果汁 | D. |  菜刀生锈 |
2.实验室制取H2有以下步骤:①连接好装置;②向试管中小心放入几粒锌;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥检验氢气的纯度.以上操作按由先至后的顺序排列正确的是( )
| A. | ①②③④⑤⑥ | B. | ①④②③⑥⑤ | C. | ①③②④⑥⑤ | D. | ③①④②⑤⑥ |
19.甲.乙两种化合物都只含X.Y两种元素,甲.乙中X元素的质量分数分别为a%和b%(a%<b%).已知甲的化学式为XY,则乙的化学式可能为( )
| A. | X2Y | B. | XY2 | C. | X2Y3 | D. | X2Y5 |
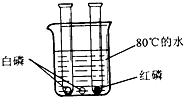 为了探究燃烧的条件,小军查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃.他设计了如图所示的实验装置.将分别盛有少量白磷和少量红磷的两支试管,放入到盛水的烧杯中,另将少量白磷直接投入到烧杯的水中.观察到的实验现象如下:①试管中的白磷燃烧,产生大量的白烟;②试管中的红磷不燃烧;③烧杯中的白磷不燃烧.
为了探究燃烧的条件,小军查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃.他设计了如图所示的实验装置.将分别盛有少量白磷和少量红磷的两支试管,放入到盛水的烧杯中,另将少量白磷直接投入到烧杯的水中.观察到的实验现象如下:①试管中的白磷燃烧,产生大量的白烟;②试管中的红磷不燃烧;③烧杯中的白磷不燃烧.