题目内容
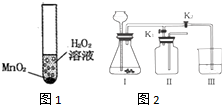 科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰 (MnO2)粉末如图1,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:
科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰 (MnO2)粉末如图1,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:| 实验次数 | 1 | 2 | 3 | 4 |
| H2O2溶液的溶质质量分数 | 1% | 5% | 10% | 15% |
| MnO2质量 | 0.2克 | 0.2克 | 0.2克 | 0.2克 |
| 气泡产生的速度 | + | ++ | +++ | ++++ |
(2)为了检验产生的气体是否为氧气,请你写出检验的方法:
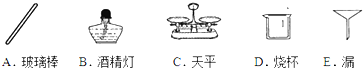
(3)实验完毕,可利用过滤法回收剩余溶液中的二氧化锰粉末.在过滤过程中,下列仪器不需要的有
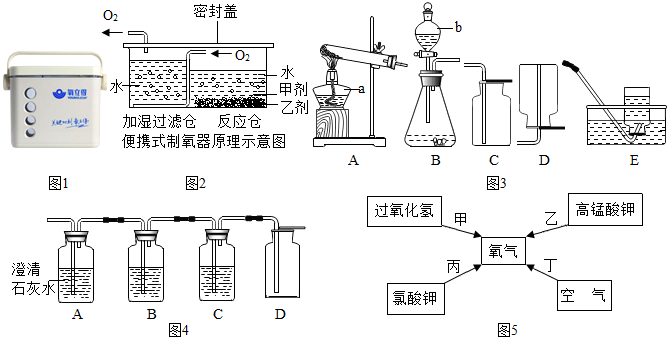
(4)如图是实验室制取、收集有关气体的装置图.请按要求回答下列问题:
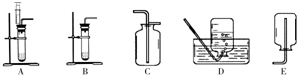
①用双氧水制取氧气的文字表达式为
③用发生装置A或B制取氧气时,A与B相比,A的优点是
④实验室制取二氧化碳组装仪器时连接玻璃管和橡皮管的方法是先把玻璃管口
(5)该小组设计了如图2所示的实验装置,既可用于制取气体,又可用于探究物质性质.
①当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是
a.大理石与稀盐酸反应制取二氧化碳 b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1时,可以利用工、Ⅲ装置制得二氧化碳并验证其性质.实验室制取二氧化碳的文字表达式是
考点:影响化学反应速率的因素探究,混合物的分离方法,仪器的装配或连接,氧气的制取装置,氧气的收集方法,氧气的检验和验满,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)通过分析实验中所给数据进行解答;
(2)根据氧气的助燃性进行解答;
(3)过滤中用到的仪器有玻璃棒、烧杯、漏斗、滤纸、铁架台等,据此进行解答.
(4)①根据化学方程式的书写步骤书写用双氧水制取氧气的化学方程式;
②要收集氧气,根据氧气的溶解性和密度来回答.
③比较发生装置的优点,要从操作的便利方面考虑.
④根据连接仪器的方法解答;
(5)
①根据发生装置和收集方法的特点分析;
②根据二氧化碳能与水发生反应产生碳酸,显酸性回答.
(2)根据氧气的助燃性进行解答;
(3)过滤中用到的仪器有玻璃棒、烧杯、漏斗、滤纸、铁架台等,据此进行解答.
(4)①根据化学方程式的书写步骤书写用双氧水制取氧气的化学方程式;
②要收集氧气,根据氧气的溶解性和密度来回答.
③比较发生装置的优点,要从操作的便利方面考虑.
④根据连接仪器的方法解答;
(5)
①根据发生装置和收集方法的特点分析;
②根据二氧化碳能与水发生反应产生碳酸,显酸性回答.
解答:解:(1)由题目中的数据可知,在二氧化锰的量一定的情况下,过氧化氢溶液的溶质质量分数越大,气泡产生的速度越快,所以该实验研究的问题是过氧化氢分解的速度与双氧水溶液的浓度的关系;
(2)因为氧气具有助燃性,用带火星的木条检验产生的气体是否为氧气.检验的方法:将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气;
(3)过滤中用到的仪器有玻璃棒、烧杯、漏斗、滤纸、铁架台等,因不需要称量和加热,故不需要天平和酒精灯.
(4)①用双氧水制氧气的化学方程式为:2H2O2
2H2O+O2↑
②而因为氧气密度比空气大,不易溶于水,故采用向上排空气法或排水法收集,因为氧气密度比空气大应正放;
③A装置多了一个溶液添加装置,可以随时补充反应所需双氧水,控制反应速率
④连接时应先把玻璃管口湿润然后稍稍用力即可把玻璃管插入胶皮管.
(5))
①当打开K1、关闭K2时,利用I、Ⅱ装置,可制取的气体是固液常温型的气体制取及该气体的密度比空气小;锌与稀硫酸反应制取氢气的发生装置特点属于固液常温型,且氢气的密度比空气小,故选择②;
②实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能与水发生反应产生碳酸,显酸性,可以利用紫色的石蕊试液变成红色进行证明.
答案:
(1)过氧化氢溶液的浓度;
(2)将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气;
(3)BC
(4)yi52H2O2
2H2O+O2↑
②C 正放
③可以随时补充反应所需双氧水,控制反应速率
④湿润
(5)
①b
②CaCO3+2HCl=CaCl2+H2O+CO2↑ 紫 色的石蕊试液
(2)因为氧气具有助燃性,用带火星的木条检验产生的气体是否为氧气.检验的方法:将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气;
(3)过滤中用到的仪器有玻璃棒、烧杯、漏斗、滤纸、铁架台等,因不需要称量和加热,故不需要天平和酒精灯.
(4)①用双氧水制氧气的化学方程式为:2H2O2
| ||
②而因为氧气密度比空气大,不易溶于水,故采用向上排空气法或排水法收集,因为氧气密度比空气大应正放;
③A装置多了一个溶液添加装置,可以随时补充反应所需双氧水,控制反应速率
④连接时应先把玻璃管口湿润然后稍稍用力即可把玻璃管插入胶皮管.
(5))
①当打开K1、关闭K2时,利用I、Ⅱ装置,可制取的气体是固液常温型的气体制取及该气体的密度比空气小;锌与稀硫酸反应制取氢气的发生装置特点属于固液常温型,且氢气的密度比空气小,故选择②;
②实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能与水发生反应产生碳酸,显酸性,可以利用紫色的石蕊试液变成红色进行证明.
答案:
(1)过氧化氢溶液的浓度;
(2)将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气;
(3)BC
(4)yi52H2O2
| ||
②C 正放
③可以随时补充反应所需双氧水,控制反应速率
④湿润
(5)
①b
②CaCO3+2HCl=CaCl2+H2O+CO2↑ 紫 色的石蕊试液
点评:本题主要考查了影响过氧化氢反应速度的因素、氧气的助燃性以及过滤中的注意事项等.通过对比实验,在分析实验数据的基础上得到正确结论,是对学生分析能力的考查.考查了实验室制取气体的发生装置、收集方法的选择以及气体的性质检验,可依据气体发生装置、收集方法的依据及气体的性质逐一分析.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
 图为A、B、C在水中的溶解度曲线图:
图为A、B、C在水中的溶解度曲线图: