题目内容
6.某研究性学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如表(已知石灰石样品中含有的杂质不溶于水,不与稀盐酸发生反应).根据实验数据计算:| 实验 次数 | 加入稀盐酸的质量/g | 剩余固体 的质量/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | 6.8 |
| 4 | 20 | x |
②样品中碳酸钙的质量分数是66%.
③求盐酸中溶质的质量分数(请写出计算过程).
分析 ①根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为6.8;
②根据图表数据可知,完全反应后,剩余固体物质的质量为6.8g,石灰石样品的质量减去剩余固体物质的质量就是样品中碳酸钙的质量,然后根据质量分数公式计算即可;
③根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,说明20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应.根据碳酸钙与盐酸反应的化学方程式和第1次完全反应中碳酸钙的质量,即可计算出第一次参与反应的HCl质量,然后根据溶质的质量分数公式计算即可.
解答 解:①根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为6.8;
②样品中碳酸钙的质量分数为:$\frac{20g-6.8g}{20g}$×100%=66%;
③由题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
设第一次参与反应的HCl质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
5g x
$\frac{100}{5g}$=$\frac{73}{x}$
x=3.65g
盐酸中溶质的质量分数为:$\frac{3.65g}{20g}$×100%=18.25%.
答:盐酸中溶质的质量分数为18.25%.
故答案为:①6.8;
②66%;
③18.25%.
点评 本题主要考查学生利用化学方程式和溶质的质量分数公式进行计算的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质组成的混合液中,充分反应后过滤,将滤渣放入稀盐酸里,有气泡产生.则下列情况不可能存在的是( )
| A. | 滤渣是Ag、Cu、Mg | |
| B. | 滤液中一定含有Zn2+、Mg2+ 和 NO3- | |
| C. | 滤渣是Ag、Cu、Zn | |
| D. | 滤液中一定没有Cu2+、Ag+ |
11.物质的性质决定用途,下列说法错误的是( )
| A. | 氯化钠可用于配制生理盐水 | |
| B. | 氧气可用于火箭燃料的助燃剂 | |
| C. | 烧碱可用于改良酸性土壤 | |
| D. | 稀盐酸可用于清除铁制品表面的铁锈 |
18.下列变化中属于物理变化的是( )
| A. | 百炼成钢 | B. | 海水晒盐 | C. | 煤气中毒 | D. | 光合作用 |
16.下列是生活中常见的一些现象,其中属于物理变化的是( )
| A. | 石蜡熔化 | B. | 食物腐烂 | C. | 木炭加热后燃烧 | D. | 燃放烟花炮竹 |
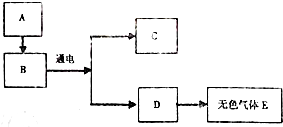 已知A-E均为初中化学常见的物质.其中A、B是组成元素相同的无色液体,E是能使澄清的石灰水变浑浊的气体;根据如图所示的转化关系(图中反应条件部分已略去),请回答
已知A-E均为初中化学常见的物质.其中A、B是组成元素相同的无色液体,E是能使澄清的石灰水变浑浊的气体;根据如图所示的转化关系(图中反应条件部分已略去),请回答 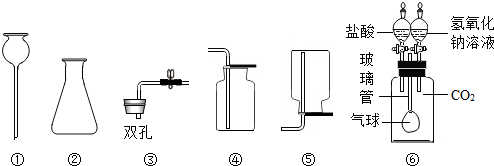
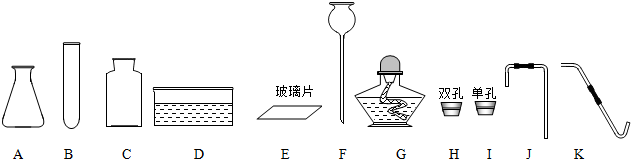
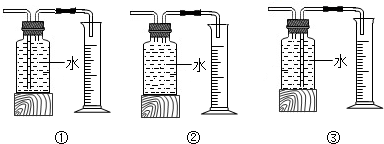
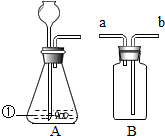 图是实验室制取二氧化碳的常用装置,请按要求填空:
图是实验室制取二氧化碳的常用装置,请按要求填空: