题目内容
将锌片和铁片同时放入硫酸铜溶液中,充分反应后,锌仍有剩余,则此时溶液中大量存在的阳离子是 将溶液过滤后,滤纸上除锌外还有 .
考点:金属的化学性质
专题:金属与金属材料
分析:根据金属与盐反应的条件判断,排在前面的金属可以把排在后面的金属从其盐溶液中置换出来.锌优先和硫酸铜反应生成硫酸锌和铜,铁和硫酸铜反应生成硫酸亚铁和铜.
解答:解:锌优先和硫酸铜反应生成硫酸锌和铜,因为锌过量,铁不会和硫酸铜反应生成硫酸亚铁和铜.所以反应后的溶液中的溶质只有硫酸锌,过滤后滤纸上的金属单质为铜、铁和锌三种.
故答案为:Zn2+;铜、铁.
故答案为:Zn2+;铜、铁.
点评:掌握金属的活动性顺序表,记住排在前面的金属可以把排在后面的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
高铁酸钾K2FeO4是一种高效水处理剂,其铁元素的化合价为( )
| A、-4 | B、+2 | C、+4 | D、+6 |
氧气由( )
| A、氧元素组成 |
| B、氧原子构成 |
| C、两个氧元素组成 |
| D、两个氧原子构成 |
在硫酸锌和硫酸铜混合液中加入过量铁粉充分反应后,过滤,留在滤纸上的是( )
| A、Cu |
| B、Zn |
| C、Zn Cu |
| D、Fe Cu |
一杯10℃的硝酸钾溶液,能证明它是饱和溶液的方法是( )
| A、蒸发5g水有固体溶质析出 |
| B、加入少许硝酸钾晶体,晶体不减少 |
| C、把溶液降温至0℃有固体溶质析出 |
| D、上述三种方法都行 |

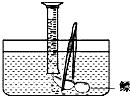 小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占
小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占