题目内容
2.工业上,高温锻烧石灰石(主要成分CaCO3)可得到生石灰(CaO)和二氧化碳,锻烧250t含碳酸钙80%的石灰石(杂质不参与反应),生成二氧化碳的质量为多少?分析 由参加反应的石灰石的质量、石灰石中碳酸钙的质量分数,由反应的化学方程式列式计算出生成二氧化碳的质量即可.
解答 解:生成二氧化碳的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
250t×80% x
$\frac{100}{44}=\frac{250t×80%}{x}$ x=88t.
答:生成二氧化碳的质量为88t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列符号中,元素符号的书写正确的是( )
| A. | 钙:CA | B. | 铝:aL | C. | 镁:mg | D. | 铁:Fe |
14.下列变化中,前者属于物理变化,后者属于化学变化的是( )
| A. | 食物腐烂,活性炭净化水 | B. | 碘升华,小白鼠呼吸 | ||
| C. | 实验室制氢气,铁生锈 | D. | 自来水用氯气杀菌,工业制氧气 |
11.依据所学知识区分下列各组物质,其方案都正确的是( )
| A | B | C | D | |
| 物 质 | 氯酸钾和 五氧化二磷 | 氮气和二氧化碳 | 高锰酸钾和二氧化锰 | 水和过氧化氢溶液 |
| 第一方案 | 观察颜色 | 燃着的木条 | 观察颜色 | 分别加入二氧化锰 |
| 第二方案 | 加入二氧化锰 | 澄清石灰水 | 加入适量的水 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
 、
、 、
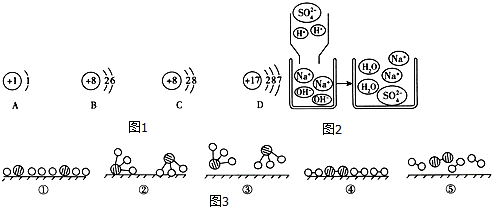
、 分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用
分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用 表示)合成氨的过程简化为图3中的五个步骤,请按照正确的步骤进行排序⑤④①②③(填序号).
表示)合成氨的过程简化为图3中的五个步骤,请按照正确的步骤进行排序⑤④①②③(填序号).