题目内容
4.某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分进行下面的实验.请你与他们一起完成以下探究活动:
【对固体猜想】
猜想I:全部是Na2CO3,
猜想Ⅱ:全部是NaOH
猜想Ⅲ:
【实验和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液 | 现象B |
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色酚酞试液变红色,则白色沉淀为CaCO3(填化学式),该实验不能 (填“能”或“不能”)说明样品中有NaOH.
分析 【对固体猜】氢氧化钠和空气中二氧化碳反应生成碳酸钠和水,所以有三种情况.
【实验和推断】
(1)碳酸钠与盐酸反应能够生成二氧化碳,而氢氧化钠和盐酸反应没有现象,若滴加稀盐酸有气体放出,则说明氢氧化钠中含有碳酸钠,已经变质;
(2)碳酸钠可与氢氧化钙反应,生成碳酸钙沉淀和氢氧化钠;向反应后的溶液中滴加无色酚酞,生成的氢氧化钠能使酚酞变红色,可以据此作答;
解答 解:【对固体猜想】
氢氧化钠和空气中的二氧化碳反应生成碳酸钠和水.如果氢氧化钠部分反应,则最后固体的成分为碳酸钠和氢氧化钠;如果氢氧化钠全部参加反应,则最后固体的成分为碳酸钠.如果没有反应则最后固体的成分为氢氧化钠;
【实验和推断】
(1)向溶液中滴加稀盐酸,盐酸与碳酸钠反应,生成氯化钠、水和二氧化碳,所以若现象A为有气泡产生,则说明氢氧化钠已经变质;
(2)向溶液中滴加氢氧化钙溶液,氢氧化钙与碳酸钠反应可生成白色的碳酸钙沉淀,同时会生成氢氧化钠,而生成的氢氧化钠同样能够使酚酞变红,因此滴入酚酞变红不能说明原来溶液中含有氢氧化钠;
故答案为:猜想Ⅲ:Na2CO3和NaOH;
(1)稀盐酸(或稀硫酸等);Na2CO3+2HCl=2NaCl+H2O+CO2↑(与所选的酸对应,合理均可);
(2)CaCO3;不能.
点评 氢氧化钠易吸水而潮解,然后和二氧化碳反应生成碳酸钠而变质,因此,在探究氢氧化钠变质情况时,需要考虑到碳酸钠溶液对氢氧化钠溶液的影响.判断是否有氢氧化钠时,一定反应产物的氢氧化钠也可以使酚酞变红,学生要留意.

练习册系列答案
相关题目
14.下列分子和原子的说法正确的是( )
| A. | 原子是最小的微粒 | |
| B. | 分子可以由同种或不同种原子构成 | |
| C. | 分子和原子都是构成物质的微粒 | |
| D. | 分子和原子的本质区别在于是否可分 |
19.在化学反应aC2H6+bO2═mCO2+nH2O中,各化学式系数之间的关系正确的是( )
| A. | 2a=m | B. | m=a | C. | n=a | D. | b=m+a |
9.下列属于混合物的是( )
| A. | 葡萄糖 | B. | 镁条完全燃烧后的生成物 | ||
| C. | 冰红茶 | D. | 氢氧化钠 |
16.下列反应属于化合反应的是( )
| A. | 氢气+氧气$\stackrel{点燃}{→}$水 | B. | 水$\stackrel{通电}{→}$氧气+氢气 | ||
| C. | 碳酸→水+二氧化碳 | D. | 氢气+氧化铜$\stackrel{高温}{→}$铜+水 |
13.两种物质发生反应的微观示意图如图所示,下列说法正确的是( )


| A. | 反应前后元素的化合价一定改变 | B. | 该反应属于分解反应 | ||
| C. | 反应前后原子的数目发生改变 | D. | 该图可示意CO与O2的反应 |
14.在天平的两个托盘上各放一只等质量的烧杯,烧杯中盛有等质量的同一种盐酸,此时天平保持平衡.在天平左右两端分别加入等质量的金属铁和锌,充分反应后铁无剩余,则以下判断正确的是( )
| A. | 锌一定无剩余 | B. | 天平平衡 | C. | 天平向右偏 | D. | 酸一定消耗完了 |
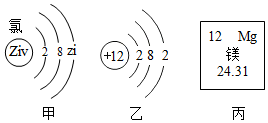 仔细观察如图并根据图示回答问题:
仔细观察如图并根据图示回答问题: