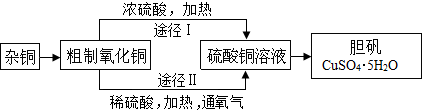
题目内容
18.下列设计的实验方案中(括号中为方法或试剂),你认为可行的是( )| A. | 验证铁、铜、银的金属活动性顺序(硫酸亚铁溶液、硝酸铜溶液、银丝) | |
| B. | 区分二氧化锰和氧化铁两种固体粉末(观察颜色) | |
| C. | 除去二氧化碳中混有少量的一氧化碳(通过灼热的氧化铜) | |
| D. | 分离氧化钙中混有的碳酸钙粉末(加水溶解,过滤) |
分析 铁比铜活泼,铜比银活泼;
二氧化锰是黑色粉末,氧化铁是红色粉末;
高温条件下,一氧化碳和氧化铜反应生成铜和二氧化碳;
水和氧化钙反应生成氢氧化钙.
解答 解:A、银丝伸入硫酸亚铁溶液、硝酸铜溶液中时,都无明显现象,说明银不如铁和铜活泼,但是无法检验铁和铜的活泼性;
B、二氧化锰是黑色粉末,氧化铁是红色粉末,通过观察颜色可以区分二氧化锰粉末和氧化铁粉末;
C、高温条件下,一氧化碳和氧化铜反应生成铜和二氧化碳,可以通过灼热的氧化铜除去二氧化碳中混有少量的一氧化碳;
D、因为水能和氧化钙反应生成氢氧化钙,因此不能用加水溶解,过滤的方法分离氧化钙中混有的碳酸钙粉末.
故选:BC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
8.下列实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 现 象 | 结 论 |
| A | 向盐酸中加入氢氧化钠溶液 | 无明显现象 | 不发生化学反应 |
| B | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性 |
| C | 铝丝、铁丝分别伸入硫酸铜溶液中 | 铝丝、铁丝上均有固体附着 | 金属的活动性顺序为Al>Fe>Cu |
| D | 在某固体中滴加稀盐酸 | 有气泡产生 | 该固体一定是碳酸盐 |
| A. | A | B. | B | C. | C | D. | D |
3.看图回答下列问题:
(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色.判断:①A中产生的气体是氢气.C中的氧化铜由黑色变为红色,反应前后(用符号填充)H,Cu元素的化合价发生了变化.
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
①写出实验室制CO2的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
| A | B | C | D | E | F | |
| 装置图 | 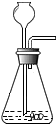 | 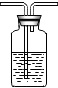 | 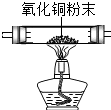 | 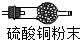 | 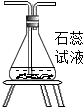 | 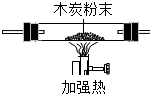 |
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
| 实验 要求 | 制CO2 | 证明CO2与H2O化合 | CO2→CO | CO还原性 | 除去混和气体 |
| 装置 编号 | A | E | F | C | B |
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
10.“物质的量”是国际单位制中的一个基本物理量,有关说法正确的是( )
| A. | 18gH2O含有3mol原子 | |
| B. | 1mol CO2中约含6.02×1023个氧原子 | |
| C. | 0.5molO2约含6.02×1023个氧 | |
| D. | CO的摩尔质量是28g |