题目内容
5.某钙片中含有碳酸钙,试着分别求出A.碳酸钙的相对分子质量:
B. 碳酸钙中碳氧两种元素的质量比:
C.碳酸钙中钙元素的质量分数:
D.若钙片中含钙10%则该钙片中碳酸钙的质量分数为多少?
E.10g此钙片中所含钙元素,与多少氧化钙所含钙元素质量相等?
分析 A.根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
B.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
C.根据化合物中元素的质量分数的计算方法来分析;
D.根据纯度=$\frac{不纯物中某元素的质量分数}{纯净物中该元素的质量分数}×100%$来分析;
E.根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析.
解答 解:A.碳酸钙的相对分子质量为40+12+16×3=100.故填:100;
B.碳酸钙中碳氧两种元素的质量比为:40:(16×3)=5:6;故填:5:6;
C.钙元素的质量分数=$\frac{40}{100}×100%=40%$;故填:40%;
D.该钙片中碳酸钙的质量分数为:$\frac{10%}{40%}×100%$=25%;故填:25%;
E.设氧化物的质量为x,则
x×$\frac{40}{56}×100%$=10g×10%
x=1.4g
故填:1.4g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
13.下列物质的用途中,是利用了其物理性质的是( )
| A. | 氧气用于医疗急救 | |
| B. | 酒精温度计可指示温度高低 | |
| C. | 氮气常用作保护气 | |
| D. | 石灰石可与盐酸反应生成二氧化碳气体 |
14.从100克10%的NaCl溶液中取出10克,那么剩下的90克NaCl的溶液中溶质质量分数是( )
| A. | 1% | B. | 90% | C. | 10% | D. | 11.1% |
15.下列实验现象中描述正确的是( )
| A. | 镁条燃烧发出耀眼的强光,生成白色的氧化镁 | |
| B. | 红磷在氧气中剧烈燃烧,产生大量的白雾 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰 | |
| D. | 水电解时生成的氧气和氢气的体积比约为1:2 |
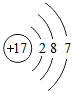 如图所示是氯原子的结构示意图.核电荷数为17,核外有3个电子层,氯原子在化学反应中易得到(填“得到”或“失去”)电子.
如图所示是氯原子的结构示意图.核电荷数为17,核外有3个电子层,氯原子在化学反应中易得到(填“得到”或“失去”)电子.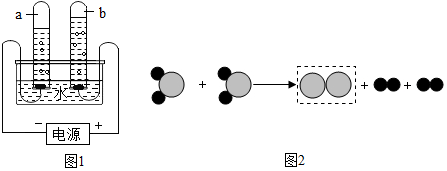
 ”表示两种不同原子.该反应属于分解(填基本反应类型)反应.
”表示两种不同原子.该反应属于分解(填基本反应类型)反应.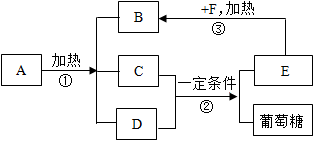 如图表示某些物质间转化关系(“→”表示物质之间存在的转化关系).A、B、F均为固体,A为绿色固体,F是一种常见金属;C是常温下一种最常见的液体; E为无色气体;C和D的反应是自然界中最重要的反应.
如图表示某些物质间转化关系(“→”表示物质之间存在的转化关系).A、B、F均为固体,A为绿色固体,F是一种常见金属;C是常温下一种最常见的液体; E为无色气体;C和D的反应是自然界中最重要的反应.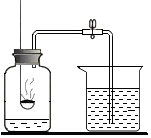 在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹.(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹.(实验装置如图所示)回答下列问题: