题目内容
3.一个碳12原子质量的十二之一是1.66×10-27kg,一个氧原子的质量为2.657×10-26kg,求氧原子的相对原子质量.分析 根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,结合题意进行分析解答即可.
解答 解:一个碳12原子质量的十二之一是1.66×10-27kg,一个氧原子的质量为2.657×10-26kg,则氧原子的相对原子质量为$\frac{2.657×1{0}^{-26}kg}{1.66×1{0}^{-27}kg}$≈16.
答:氧原子的相对原子质量为16.
点评 本题难度不大,掌握原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$并能灵活运用是正确解答本题的关键.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
18.下列现象的微观解释中,不正确的是( )
| A. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| B. | 用警犬搜救地震中被埋人员--分子在不断运动 | |
| C. | 用水银温度计测量体温--温度升高,原子间隔变大 | |
| D. | 分子可以再分,而原子不可以再分 |
12.下列是实验室中化学药品的鉴别方法,正确的是( )
| A. | 品尝:白醋和糖水 | B. | 肥皂水:硬水和软水 | ||
| C. | 二氧化锰:水和过氧化氢溶液 | D. | 带火星的木条:氮气和二氧化碳 |
13.下列能保持氧气化学性质的是( )
| A. | O | B. | O2- | C. | O2 | D. | 2O |
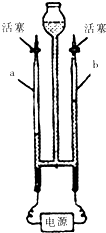 如图是电解水实验的示意图:
如图是电解水实验的示意图: