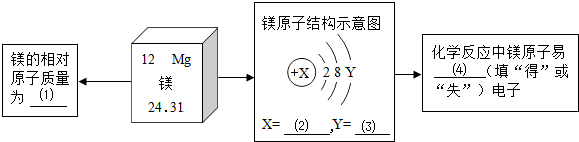
题目内容
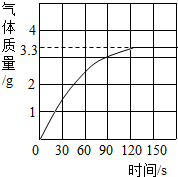 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙(CaCO3)和氢氧化镁(Mg(OH)2).他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙(CaCO3)和氢氧化镁(Mg(OH)2).他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.(1)从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是
(2)水垢中碳酸钙的质量分数是多少?(CaCO3+2HCI═CaCI2+H2O+CO2↑)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据反应产生气体的情况图,当反应到120s时放出二氧化碳气体达最大值,为3.3g;
(2)放出二氧化碳达最大值时,水垢中碳酸钙完全反应,根据反应的化学方程式,由放出二氧化碳的质量计算出样品中碳酸钙质量,碳酸钙质量与水垢样品质量比可计算水垢中碳酸钙的质量分数.
(2)放出二氧化碳达最大值时,水垢中碳酸钙完全反应,根据反应的化学方程式,由放出二氧化碳的质量计算出样品中碳酸钙质量,碳酸钙质量与水垢样品质量比可计算水垢中碳酸钙的质量分数.
解答:解:(1)由反应产生气体的情况图,可知12.5g水垢与盐酸反应后生成的二氧化碳最多是3.3g;
故答案为:3.3;
(2)设12.5g水垢中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
=
x=7.5g
水垢中碳酸钙的质量分数
×100%=60%
答:
(1)3.3
(2)水垢中碳酸钙的质量分数是60%.
故答案为:3.3;
(2)设12.5g水垢中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
| 100 |
| x |
| 44 |
| 3.3g |
x=7.5g
水垢中碳酸钙的质量分数
| 7.5g |
| 12.5g |
答:
(1)3.3
(2)水垢中碳酸钙的质量分数是60%.
点评:产生CO2气体的情况曲线折点表明此时放出气体二氧化碳达最大值,即水垢是碳酸钙完全反应.

练习册系列答案
相关题目
保持水的化学性质的最小粒子是( )
| A、水分子 |
| B、氧元素和氢元素 |
| C、氧原子和氢原子 |
| D、氢分子和氧分子 |
下列物质由离子构成的是( )
| A、蒸馏水 | B、氯化钠 |
| C、金刚石 | D、二氧化硫 |
关于化学变化中的“新物质”的解释正确的是( )
| A、自然界中不存在的物质 |
| B、与变化前的物质在颜色、状态方面有所不同的物质 |
| C、元素种类发生改变的物质 |
| D、在组成和结构上与变化前不同的物质 |
下列说法正确的是( )
| A、最外层有8个电子的粒子一定是稀有气体元素的原子 |
| B、核电荷数相同的粒子一定是同种元素的原子 |
| C、含有氧元素的化合物不一定是氧化物 |
| D、纯净物一定由同种分子构成 |
甲、乙两物质发生反应的微观示意图如图,通过观察你认为下列说法不正确的是( )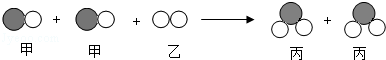
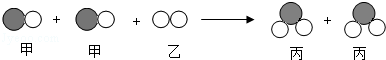
| A、该反应属于化合反应 |
| B、该反应前后原子个数保持不变 |
| C、甲和丙中同种元素的化合价均相等 |
| D、参加反应的甲和乙的质量和等于生成的丙的质量 |