题目内容
某化学小组的同学为了测定某矿山石灰石中的碳酸钙的质量分数,取石灰石样品和足量稀盐酸在烧杯中反应(假设石灰石样品中的杂质不跟稀盐酸反应,也不溶于水).有关实验数据如下表
(1)反应中生成二氧化碳的质量为 g,根据 得出.
(2)求该石灰石中碳酸钙的质量分数.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
(2)求该石灰石中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
解答:解:
(1)根据质量守恒定律,二氧化碳的质量为:150g+12g-157.6g=4.4g.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
=
x=10g
此石灰石中碳酸钙的质量分数为:
×100%≈83.3%
答案:
(1)4.4 质量守恒定律
(2)此石灰石中碳酸钙的质量分数为83.3%
(1)根据质量守恒定律,二氧化碳的质量为:150g+12g-157.6g=4.4g.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g
此石灰石中碳酸钙的质量分数为:
| 10g |
| 12g |
答案:
(1)4.4 质量守恒定律
(2)此石灰石中碳酸钙的质量分数为83.3%
点评:本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
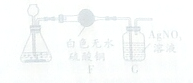
某化学小组的同学利用混有少量CO2的CO气体还原氧化铜,并验证反应后的气体产物.实验室现有下图所示实验装置(所有装置均可重复使用).按气体从左到右的方向,装置连接顺序正确的是( )

| A、甲→乙→丙→丁 |
| B、甲→丙→乙→丁 |
| C、乙→甲→丙→乙→丁 |
| D、乙→甲→丙→甲→丁 |
氢气与氧气的混合气体20g,使之充分燃烧后生成9g水,则混合气体中含有氧气质量可能是( )
| A、9g | B、8g |
| C、10g | D、19g |
“珍爱生命,远离毒品”.冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N).有关甲基苯丙胺的说法正确的是( )
| A、甲基苯丙胺中碳、氢、氮元素的质量比为10:15:1 |
| B、甲基苯丙胺由碳、氢、氮元素组成 |
| C、甲基苯丙胺中氢元素质量分数最低 |
| D、燃烧只生成二氧化碳和水 |
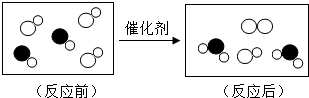 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A、此反应不属于置换反应 |
| B、原子在化学变化中是不可分的 |
| C、图中反应物全部是化合物 |
| D、参加反应的两种分子的个数比为2:3 |
 向一定质量CaCl2和HCl混合溶液中逐滴加入质量分数为10%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.
向一定质量CaCl2和HCl混合溶液中逐滴加入质量分数为10%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.