题目内容
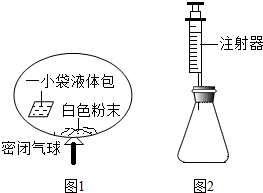
7.某研究小组对自动充气气球(示意图如图1)进行下列探究.[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为检验气体是二氧化碳,可选用氢氧化钙溶液(填试剂名称)、
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈酸性.
探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠.
[设计并进行实验]
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确(填“正确”或“不正确”)、
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
| 实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
| 名称 | 质量/g | ||
| ① | 碳酸氢钠 | 0、10 | V1 |
| ② | 碳酸钠 | 0、10 | V2 |
| ③ | 白色粉末 | x | V1 |
[分析并得出结论]
(5)白色粉末是碳酸氢钠、
分析 (1)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
(2)根据pH小于7的溶液显酸性进行分析;
(3)根据碳酸钙难溶于水进行分析;
(4)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,控制变量法的正确操作方法进行分析;
(5)根据表中的数据进行分析.
解答 解:(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以为检验气体是二氧化碳,可选用氢氧化钙溶液;
(2)pH小于7的溶液显酸性,所以室温时,用pH试纸测得溶液的pH=3的溶液呈酸性;
(3)碳酸钙难溶于水,所以将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确;
(4)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,碳酸氢钠、碳酸钠的质量都是0.1g,为了形成对比,所以x的质量也是0.1g,每84份质量的碳酸氢钠会生成44份质量的二氧化碳,每106份质量的碳酸钠会生成44份质量的二氧化碳,所以V1>V2;
(5)根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
故答案为:(1)氢氧化钙溶液;
(2)酸;
(3)不正确;
(4)NaHCO3+HCl=NaCl+H2O+CO2↑,0.1,>;
(5)碳酸氢钠.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.小金利用图示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略).
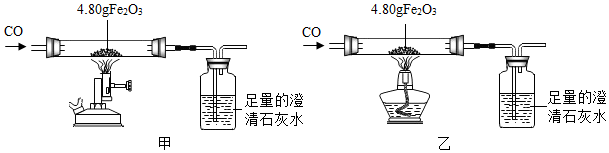
(1)从实验安全角度考虑,图示装置还应采取的改进措施是导管后放点燃的酒精灯或在导管后扎气球.
(2)完全反应后,两组的生成物均为黑色粉未(纯净物),分别用两组生成物进行以下实验:
①甲组的黑色粉末与稀盐酸反应的化学方程式是Fe+2HCl═FeCl2+H2↑.
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4.他又发现m2恰好为4.64g,这可成为支持上述猜想的新证据.
(3)甲、乙两组实验说明温度对CO和Fe2O3反应影响,且均体现出CO的还原性(填写化学性质).

(1)从实验安全角度考虑,图示装置还应采取的改进措施是导管后放点燃的酒精灯或在导管后扎气球.
(2)完全反应后,两组的生成物均为黑色粉未(纯净物),分别用两组生成物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 称量黑色粉末质量/g | m1 | m2 |
| 2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
| 3 | 取黑色粉未,加入稀盐酸 | 全部溶解,有大量气泡 | 无明显现象 |
| 4 | 取黑色粉末,加入足量CuSO4溶液 | 有红色物质生成 | 无明显现象 |
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4.他又发现m2恰好为4.64g,这可成为支持上述猜想的新证据.
(3)甲、乙两组实验说明温度对CO和Fe2O3反应影响,且均体现出CO的还原性(填写化学性质).
17.下列方法能区分氧气和二氧化碳两瓶气体的是( )
| A. | 闻气味 | B. | 观察颜色 | ||
| C. | 倒入适量氢氧化钠溶液 | D. | 将燃着的木条伸入集气瓶中 |
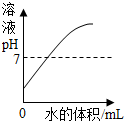 向盐酸中加入水
向盐酸中加入水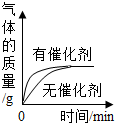
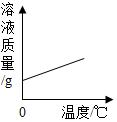 将饱和石灰水升温
将饱和石灰水升温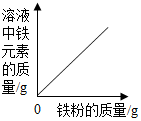 向一定量的稀盐酸中加入铁粉
向一定量的稀盐酸中加入铁粉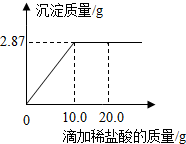 为测定某硝酸银溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(计算结果均保留1位小数)
为测定某硝酸银溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(计算结果均保留1位小数)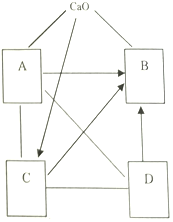 如图中A、B、C、D分别表示初中常见不同类别的四种物质,A由两种元素组成,图中用“-”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,(图中部分反应需在溶液中进行),请回答下列问题
如图中A、B、C、D分别表示初中常见不同类别的四种物质,A由两种元素组成,图中用“-”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,(图中部分反应需在溶液中进行),请回答下列问题 如图是一瓶铝盐溶液,请用正确的化学用语填空:
如图是一瓶铝盐溶液,请用正确的化学用语填空: