题目内容
17.下列叙述正确的是( )| A. | 卢瑟福建立的“卢瑟福模型”认为电子像云雾一样出现在原子核周围 | |
| B. | 汤姆生建立的“汤姆生模型”认为原子核像太阳,电子像行星绕原子核运行 | |
| C. | 玻尔建立的“分层模型”认为电子在原子核周围分层运动 | |
| D. | 现代科学家认为电子像西瓜籽似地嵌在原子中 |
分析 A、根据卢瑟福建立的“卢瑟福模型”是发现原子核,原子大部分体积是空的,电子围绕带正电的原子核随意动转进行解答;
B、根据汤姆生建立的“汤姆生模型”即“西瓜模型”正电荷是西瓜肉,电子是西瓜籽进行解答;
C、根据波尔建立的“分层模型”认为电子在原子核周围分层运动进行解答;
D、根据现代科学家认为电子是在原子核周围分层运动进行解答
解答 解:A、卢瑟福建立的“卢瑟福模型”是发现原子核,原子大部分体积是空的,电子围绕带正电的原子核随意动转,故A错误;
B、汤姆生建立的“汤姆生模型”即“西瓜模型”正电荷是西瓜肉,电子是西瓜籽,故B错误;
C、波尔建立的“分层模型”认为电子在原子核周围分层运动,故C正确;
D、现代科学家认为电子是在原子核周围分层运动,故D错误.
故选:C
点评 了解人类认识物质世界的历史,对培养科学探究精神和科学态度有着不可忽视的作用.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
8.为了研究锌片、铁片和铜片的金属活动性强弱关系,应选择下列中的( )
| A. | 稀硫酸溶液 | B. | 碳酸钙溶液 | C. | 硝酸钾溶液 | D. | 氢氧化钠溶液 |
5.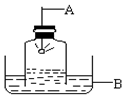 做空气中氧气含量测定的实验装置如图(A是燃烧匙;B是水槽,水槽内盛的是水).下列有关说法正确的是( )
做空气中氧气含量测定的实验装置如图(A是燃烧匙;B是水槽,水槽内盛的是水).下列有关说法正确的是( )
 做空气中氧气含量测定的实验装置如图(A是燃烧匙;B是水槽,水槽内盛的是水).下列有关说法正确的是( )
做空气中氧气含量测定的实验装置如图(A是燃烧匙;B是水槽,水槽内盛的是水).下列有关说法正确的是( )| A. | 选用足量的红磷是因为反应可以耗尽O2,生成固态的P2O5 | |
| B. | 燃烧匙中的红磷可以换成硫或木炭 | |
| C. | 燃烧匙中的红磷越多,水位上升越高 | |
| D. | 本实验可以证明空气含有N2、O2、CO2和稀有气体 |
12.凉开水不宜用来养鱼,是因为凉开水中缺少( )
| A. | 氧元素 | B. | 氧分子 | C. | 氧原子 | D. | 氧离子 |
9.下列反应中属于化合反应的是( )
| A. | 铁丝在氧气中燃烧 | |
| B. | 石蜡在空气中燃烧生成二氧化碳和水 | |
| C. | 分离液态空气 | |
| D. | 氧化汞加热分解生成汞和氧气 |
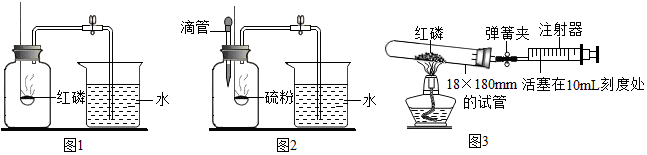
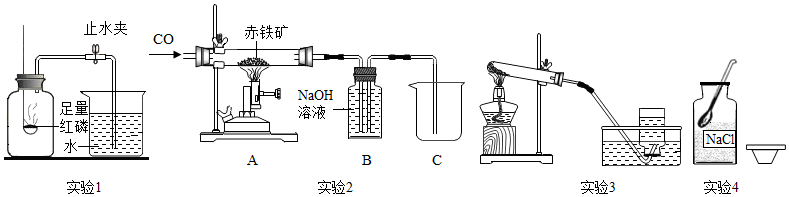
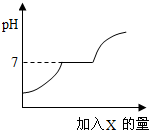 科学探究活动中,老师介绍了一些科学知识:
科学探究活动中,老师介绍了一些科学知识: