题目内容
11.有一包固体A和黑色粉末B混合加热后产生另一白色固体C和无色、无味的气体D,D可使带火星的木条复燃.把淡黄色粉末E加热放入盛D的集气瓶里,发出蓝紫色火焰,生成一种有刺激性气味F.则A、B、C、D、E、F各是什么物质?(1)A:氯酸钾B:二氧化锰C:氯化钾D:氧气E:硫粉F:二氧化硫
(2)写出A和B混合加热产生白色固体C和气体D的文字表达式:氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气.
(3)写出淡黄色粉末C在气体D中燃烧的文字表达式:硫+氧气 $\stackrel{点燃}{→}$ 二氧化硫.
分析 根据D气体可使带火星木条复燃,所以D为氧气,淡黄色的粉末E能在氧气中燃烧,且发出紫色火焰,生成有刺激性气味的气体F,所以E为硫粉,F为二氧化硫,固体A和黑色粉末B能够生成氧气和白色固体C,所以A氯酸钾,B为二氧化锰,C是氯化钾,然后将推出的各种物质代入转化关系中验证即可.
解答 解:D气体可使带火星木条复燃,所以D为氧气,淡黄色的粉末E能在氧气中燃烧,且发出紫色火焰,生成有刺激性气味的气体F,所以E为硫粉,F为二氧化硫,固体A和黑色粉末B能够生成氧气和白色固体C,所以A氯酸钾,B为二氧化锰,C是氯化钾,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,氧气可以使带火星的木条复燃,硫和氧气在点燃的条件下生成二氧化硫,发出紫色火焰,推出的各种物质均满足题中的转化关系,推导正确,所以A是氯酸钾,B是二氧化锰,C是氯化钾,D是氧气,E是硫粉,F是二氧化硫.
故答案为:氯酸钾,二氧化锰,氯化钾,氧气,硫粉,二氧化硫.
(2)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,所以A和B混合加热产生白色固体C和气体D的文字表达式为:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(3)硫和氧气在点燃的条件下生成二氧化硫,淡黄色粉末C在气体D中燃烧的文字表达式为:硫+氧气$\stackrel{点燃}{→}$二氧化硫.
故答案为:(1)氯酸钾;二氧化锰;氯化钾;氧气;硫粉;二氧化硫;
(2)氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气;
(3)硫+氧气 $\stackrel{点燃}{→}$ 二氧化硫.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
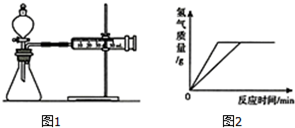 某化学学习小组为比较镁和铁的金属活动性强弱设计了如下实验方案.
某化学学习小组为比较镁和铁的金属活动性强弱设计了如下实验方案.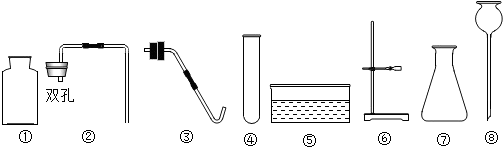

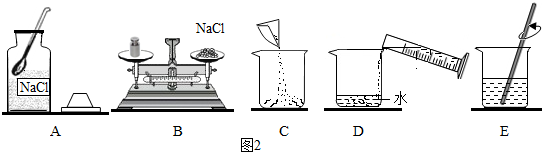
 水是一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.试回答下列问题:
水是一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.试回答下列问题: