题目内容
5.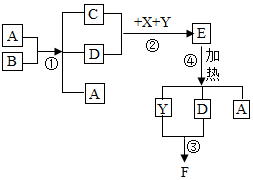 如图表示某些物质间的转化关系(部分反应条件省略).其中A为黑色固体氧化物;E为绿色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y为常见无色气体;X是常见的红色金属单质.
如图表示某些物质间的转化关系(部分反应条件省略).其中A为黑色固体氧化物;E为绿色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y为常见无色气体;X是常见的红色金属单质.请回答下列问题:
(1)F的化学式:C6H12O6.
(2)A在反应①中的作用催化作用.
(3)写出反应①、④的化学方程式:
①2H2O2$\stackrel{CuO}{=}$2H2O+O2↑;④Cu2(OH)2 CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(4)Y和D发生化合反应时生成F,但Y和D在光照和叶绿素存在条件下也可反应生成葡萄糖(C6H12O6)和O2,试分析反应物相同而生成物不同的原因是同种反应物在不同反应条件下生成物可能不同.
分析 考虑过氧化氢在氧化铜催化作用下分解生成水和氧气;
红色金属单质铜在水、氧气、二氧化碳的作用下反应生成绿色固体碱式碳酸铜,碱式碳酸铜受热分解生成氧化铜、水和二氧化碳,碱式碳酸铜和稀盐酸反应生成氯化铜、水和二氧化碳;
二氧化碳和水在光照条件下,在叶绿素中能够反应生成葡萄糖和氧气.
解答 解:因为过氧化氢在氧化铜催化作用下分解生成水和氧气;
红色金属单质铜在水、氧气、二氧化碳的作用下反应生成绿色固体碱式碳酸铜,碱式碳酸铜受热分解生成氧化铜、水和二氧化碳,碱式碳酸铜和稀盐酸反应生成氯化铜、水和二氧化碳;
二氧化碳和水在光照条件下,在叶绿素中能够反应生成葡萄糖和氧气,因此ABCDEXY分别是氧化铜、过氧化氢、氧气、水、碱式碳酸铜、铜和二氧化碳;
(1)F的化学式是C6H12O6.
(2)反应①中氧化铜的作用是催化作用,能够加快过氧化氢的分解速率.
(3)反应①、④的化学方程式为:2H2O2$\stackrel{CuO}{=}$2H2O+O2↑,Cu2(OH)2 CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(4)Y和D直接反应能生成F碳酸,但是Y和D在光照和叶绿素条件下却能生成C6H12O6和O2,从反应物、生成物等角度分析,可得出同种反应物在不同反应条件下生成物可能不同的结论.
故答案为:
(1)C6H12O6.(2)催化作用.(3)①2H2O2$\stackrel{CuO}{=}$2H2O+O2↑;④Cu2(OH)2 CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(4)同种反应物在不同反应条件下生成物可能不同.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案| A. | 生铁和钢的性质不同,是由于含碳量不同 | |
| B. | O2和O3性质不同,是由于构成它们的分子不同 | |
| C. | NaCl晶体和溶液导电性不同,是由于构成它们的离子不同 | |
| D. | 金刚石和石墨的物理性质不同,是由于碳原子的排列方式不同 |
| A. | 铜用于制造电线 | B. | 镁用于制造照明弹芯 | ||
| C. | 石墨用于制铅笔 | D. | 氢气用于填充气球 |
| A. | 磷在空气中燃烧,反应剧烈,产生大量白雾 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| C. | 铜丝在空气中灼烧,红色金属表面变黑 | |
| D. | 硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体 |
| A. | 一个偏二甲肼分子中含有一个氮分子 | |
| B. | 相对分子质量是60g | |
| C. | 碳氢氮三种元素质量比为1:4:1 | |
| D. | 偏二甲肼中氢元素的质量分数最小 |
| A. | C2H6 | B. | C2H4 | C. | C2H5OH | D. | C2H2 |
| A. | 石灰水 | B. | 铝合金 | C. | 液氧 | D. | 浓硫酸 |
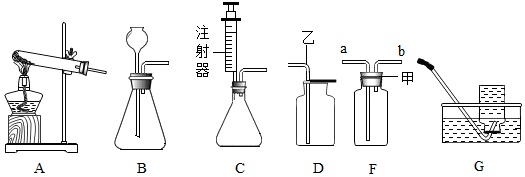
 A-G是初中常见的7种物质,它们有如下图所示的转化关系.已知A、C是无色液体,B、F、G是无色气体,其中F是绿色植物光合作用的原料,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.
A-G是初中常见的7种物质,它们有如下图所示的转化关系.已知A、C是无色液体,B、F、G是无色气体,其中F是绿色植物光合作用的原料,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.