题目内容
祁阳人爱吃辣椒,一种“朝天辣椒”:表皮鲜红有光泽,久藏不变色,辣味强烈,有“辣椒王”之称。某菜农发现自家地里种的辣椒生长迟缓、叶色淡黄,在读九年级的女儿说是缺养分,必须追加复合肥料。下列属于复合肥料的是
A.K2SO4 B.NH4Cl C.CO(NH2)2 D、NH4H2PO4
D

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案有四瓶失去标签的溶液,它们的溶质分别是①硝酸钡、②硝酸银、③氯化钠、④氯化铜,不用其他试剂就可以将它们加以鉴别,则鉴别出来的先后顺序可能是( )
A.④②③① B.①③②④ C.④①②③ D.②③①④
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)
进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的探究。
 Ⅰ.定性探究:
Ⅰ.定性探究:
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是 ,
②是CaCl2.
【收集资料】CaCl2水溶液呈中性。
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加 |
| 猜想①正确。碳酸钠与其反应的化学方程式为 |
探究二  过滤后澄清滤液中会有哪些溶质?
过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3 ;
猜想二: ;
猜想三:NaOH 。
(3)【实验验证】同学们经过交流讨论,设计以下实验方案确定滤液中溶质的 组成:
组成:
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入 溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
|
| “猜想二”成立 | |
|
| “猜想三”成立 |
Ⅱ.定量探究:
【提出问题】过滤后澄清滤液中NaOH的质量分数是多少?
【设计实验】
小明同学取100g过滤后澄清滤液于烧杯中,向烧杯中逐滴加入过量的稀盐酸,产生的气体与所加入稀盐酸质量关系如下图所示:计算过滤后澄清滤液中NaOH的质量分数是多少?(请列出计算过程)
 |

 ( ▲ )
( ▲ )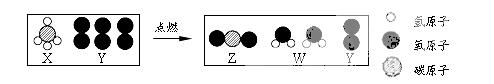
 CO2+H2O
CO2+H2O