题目内容
9.二氧化碳能产生温室效应,还能作化工原料.(1)化石燃料燃烧会产生大量的CO2,天然气(CH4)充分燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)膜分离是一种常用的分离技术.二氧化硅(SiO2)能用于制造CO2分离膜,CO2通过此膜后被氨水吸收(如图1所示),转化为可作氮肥的NH4HCO3.

①NH4HCO3固体中氮元素的质量分数为17.1%(计算结果精确到0.1%).
(3)CO2形成的超临界CO2流体可用于从香兰草豆荚粉中提取香兰素(C8H8O3)(如图2).
①香兰素的乙醇溶液中的溶剂是乙醇.
②由香兰素的乙醇溶液得到香兰素的过程中,发生的是物理变化(填物理或化学).
③以上提取香兰素的过程中,可循环使用的物质有无水乙醇和CO2.
④完全燃烧19g香兰素所生成的一氧化碳与完全燃烧23g无水乙醇(俗名酒精,C2H5OH)所生成的二氧化碳的质量相等.
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)①根据二氧化硅的化学式为SiO2,利用氧化物中氧元素的化合价及化合物中元素的正负化合价的代数和为0来计算其中硅元素的化合价;
②根据化合物中元素的质量分数进行分析;
(3)①根据溶液的组成解答;
②根据由香兰素的乙醇溶液得到香兰素的过程中没有新物质生成解答;
③根据题中信息解答;
④根据化学式进行计算即可.
解答 解:
(1)天然气的主要成分是甲烷,甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)①碳酸氢铵中氮元素的质量分数=$\frac{14}{14+1×4+12+16×3}$×100%≈17.7%;故填:+4;17.7%;
(3)①香兰素的乙醇溶液中的溶剂是乙醇;故填:乙醇;
②由香兰素的乙醇溶液得到香兰素的过程中,发生的是物理变化;
③根据图示可知可循环使用的物质有CO2,无水乙醇;故填:CO2;
④二氧化碳的质量相等也就是所含碳元素的质量相等.根据质量守恒定律可知,也就是香兰素中碳元素的质量与乙醇中碳元素的质量相等.
设乙醇的质量为x,则
19g×$\frac{12×8}{12×8+1×8+16×3}$×100%=x×$\frac{12×2}{12×2+1×6+16}$×100%
x=23g
故填:23.
答案:
(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)①17.7%
(3)①乙醇;②物理;③CO2;④23.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
| A. | 大量使用塑料购物袋 | B. | 工业和生活污水任意排放 | ||
| C. | 大量使用煤作燃料 | D. | 农业生产任意使用农药和化肥 |
| A. | H2 | B. | NO2 | C. | CO2 | D. | NO |
| A. | 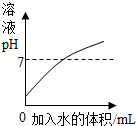 表示向稀盐酸中不断加水 表示向稀盐酸中不断加水 | |
| B. |  表示探究过氧化氢制氧气的反应中二氧化锰的作用 表示探究过氧化氢制氧气的反应中二氧化锰的作用 | |
| C. | 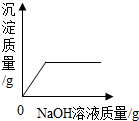 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 | |
| D. | 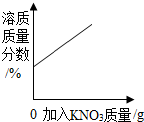 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 |
| A. | 向加碘食盐溶液中滴加淀粉,溶液变蓝 | |
| B. | 打开浓盐酸的瓶塞时,瓶口冒白雾 | |
| C. | 将铜加入到稀硫酸的溶液中,产生大量气泡 | |
| D. | 一氧化碳通入澄清石灰水中,澄清石灰水变浑浊 |
| A. | Na2CO3、稀H2SO4、稀HCl、KNO3 | B. | 稀HCl、Na2CO3、BaCl2、Na2SO4 | ||
| C. | NaOH、Na2CO3、酚酞、CaCl2 | D. | CuSO4、NaOH、KNO3、NaCl |