题目内容
写出有关二氧化碳的化学方程式
(1)实验室制取二氧化碳气体 ;
(2)有二氧化碳气体生成的分解反应 ;
(3)有二氧化碳生成的置换反应 ;
(4)有二氧化碳参与的化合反应 ;
(5)检验二氧化碳气体 ;
(6)有二氧化碳生成,但不属于以上任何一个反应类型 .
(1)实验室制取二氧化碳气体
(2)有二氧化碳气体生成的分解反应
(3)有二氧化碳生成的置换反应
(4)有二氧化碳参与的化合反应
(5)检验二氧化碳气体
(6)有二氧化碳生成,但不属于以上任何一个反应类型
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)实验室常用石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙和水,反应的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)碳酸分解生成水和二氧化碳,属于分解反应,反应的化学方程式为:H2CO3═H2O+CO2↑(合理均可).
(3)碳和氧化铜在高温条件下生成铜和二氧化碳,反应的化学方程式为C+2CuO
2Cu+CO2↑(合理均可).
(4)二氧化碳与水反应生成碳酸,属于化合反应,反应的化学方程式为:H2O+CO2═H2CO3.
(5)检验二氧化碳气体用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(6)一氧化碳与氧化铜反应生成铜和二氧化碳,不属于以上任何一个反应类型,反应的化学方程式为:CuO+CO
Cu+CO2(合理即可).
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)H2CO3═H2O+CO2↑(合理均可);
(3)C+2CuO
2Cu+CO2↑(合理均可);
(4)H2O+CO2═H2CO3;
(5)CO2+Ca(OH)2═CaCO3↓+H2O;
(6)CuO+CO
Cu+CO2(合理即可).
(2)碳酸分解生成水和二氧化碳,属于分解反应,反应的化学方程式为:H2CO3═H2O+CO2↑(合理均可).
(3)碳和氧化铜在高温条件下生成铜和二氧化碳,反应的化学方程式为C+2CuO
| ||
(4)二氧化碳与水反应生成碳酸,属于化合反应,反应的化学方程式为:H2O+CO2═H2CO3.
(5)检验二氧化碳气体用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(6)一氧化碳与氧化铜反应生成铜和二氧化碳,不属于以上任何一个反应类型,反应的化学方程式为:CuO+CO
| ||
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)H2CO3═H2O+CO2↑(合理均可);
(3)C+2CuO
| ||
(4)H2O+CO2═H2CO3;
(5)CO2+Ca(OH)2═CaCO3↓+H2O;
(6)CuO+CO
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
从100g 9%的NaCl溶液中取出10g,那么剩下的90g NaCl溶液的质量分数是( )
| A、1% | B、9% |
| C、10% | D、11.1% |
 现在一瓶未开封的浓硫酸,部分标签如表所示,
现在一瓶未开封的浓硫酸,部分标签如表所示,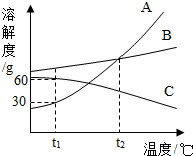 根据如图溶解度曲线回答下列问题:
根据如图溶解度曲线回答下列问题: