题目内容
19.将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄金”的组成进行了以下探究.[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;
ZnCO3高温可分解成两种氧化物.
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成作了以下三种猜想:
猜想①可能是单质:C、Zn、Cu
猜想②可能是氧化物:ZnO、CuO、Cu2O
猜想③可能是单质和氧化物组成的混合物
[论证](1)乙同学经过思考和推理后,首先排除了其中的两个猜想②③(填①②③序号),理由是因为C过量,所以可以将氧化物还原成金属;对余下的一种猜想,乙同学又排除了其中的一种物质,依据是C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)对余下的两种物质(ab代表),甲和乙同学利用下列实验方案进行验证:
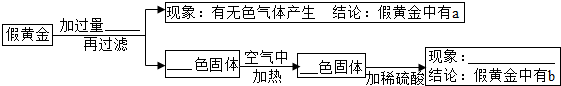
(3)写出上述实验过程中发生反应的任意一个化学方程式Zn+2HCl═ZnCl2+H2↑;
[结论与应用](4)“假黄金”的成分中a为Znb为Cu;
生活中真假黄金的鉴别,可采用的一种方法是(要求写出操作、现象和结论)加稀盐酸,能与稀盐酸反应产生气体则为假黄金,不能与稀盐酸反应则为真黄金.
分析 ZnCO3高温可分解成两种氧化物,其中一种为氧化锌,生成的氧化锌和赤铜矿(Cu2O)和过量的炭混合后,高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质,锌和铜均在铝的后面,故能全部被还原为金属,得到的锌在氢前,可与酸发生置换反应产生氢气,而铜在氢后,不能与酸发生置换反应生成氢气.
解答 解:(1)碳酸锌高温分解的产物之一是氧化锌,与氧化亚铜一起可被过量的碳完全还原为金属,不可能有氧化物存在,而碳在高温时可被氧化为二氧化碳,不可能有碳存在,所以本题答案为:②③,因为C过量,所以可以将氧化物还原成金属,C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)生成的锌在氢前,可与酸发生置换反应产生氢气,而铜在氢后,不能与酸发生置换反应生成氢气,所以可使用HCl进行验证,得红色固体,在空气中加热生成黑色固体,加稀硫酸溶解生成蓝色溶液.所以本题答案为:HCl;红色,黑色,加稀硫酸溶解生成蓝色溶液.
(3)加盐酸有气体产生,则是锌与盐酸反应,所以本题答案为:Zn+2HCl═ZnCl2+H2↑;
(4)加入盐酸有气泡产生说明含a,则a为锌,故b为铜,假黄金中含 锌,可与酸反应产生氢气,而真黄金不与酸发生置换反应,所以可采用加酸的方法验证,所以本题答案为:Zn,Cu,加稀盐酸,能与稀盐酸反应产生气体则为假黄金,不能与稀盐酸反应则为真黄金.
故答案为:
(1)②③;因为C过量,所以可以将氧化物还原成金属; C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)HCl;红色,黑色,加稀硫酸溶解生成蓝色溶液.
(3)Zn+2HCl═ZnCl2+H2↑;
(4)Zn、Cu; 加稀盐酸,能与稀盐酸反应产生气体则为假黄金,不能与稀盐酸反应则为真黄金.
点评 本题考查了金属氧化物与碳的还原反应以及常见金属的化学性质,完成此题,可以依据课本已有的知识进行知识的迁移.所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.

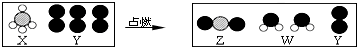
| A. | 涉及到五种物质 | B. | 反应前后分子的种类不变 | ||
| C. | 反应前后原子的种类不变 | D. | 反应前后元素种类改变 |
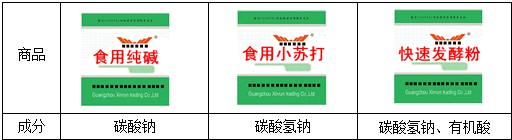
【提出问题】这种白色粉末是什么物质?
【查阅资料】通过对市场上相关产品进行调查,王霞发现了如图所示的三种商品.
【作出猜想】
猜想1:可能是食用纯碱;
猜想2:可能是食用小苏打;
猜想3:可能是快速发酵粉.
【设计实验】取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,实验结论是此粉未不是快速发酵粉,另取少量白色粉末于试管中,加入稀盐酸,有无色气体产生,王霞认为白色粉末是纯碱..
【实验反思】小明同学认为王霞同学根据上面的实验现象,不能得出白色粉末是纯碱,你若认为小明说法有道理,请用化学方程式解释不能得出结论的原因NaHCO3+HCl═NaCl+H2O+CO2↑;为了得到鉴别纯碱和小苏打的正确方法,王霞继续查找资料,发现它们有下列的性质.
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
方案1:加入CaCl2溶液,碳酸钠与之反应生成沉淀,则有沉淀生成的为碳酸钠,反之为碳酸氢钠;
方案2:20℃时,在100克水中加入12克该白色粉末,充分溶解后,如果有白色固体剩余,则为碳酸钠,否则为碳酸氢钠.
在查找资料过程中,王霞同学还发现纯碱不是碱,是由于其水溶液显碱性而得名.现要验证纯碱溶液是否显碱性,请写出用pH试纸来测其pH值的操作过程把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数.
| A. | 碳酸钙 $\stackrel{高温}{→}$氧化钙+二氧化碳 | B. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | ||
| C. | 食盐+水→食盐水 | D. | 蜡烛+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
| 序号 | 物 质 | 选用试剂 | 操作 |
| A | CO2(CO) | O2 | 点燃 |
| B | NaOH溶液(Na2CO3) | 稀盐酸 | 加入试剂至不再产生气泡 |
| C | KNO3溶液(KOH) | H2SO4溶液 | 加入适量的试剂 |
| D | Cu(Fe) | 稀硫酸 | 加入适量的试剂,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | X由碳、氢、氧三种元素组成 | B. | X可以用燃着的木条检验 | ||
| C. | X中碳、氧元素的质量比为3:4 | D. | X中碳、氧元素的化合价代数和为零 |
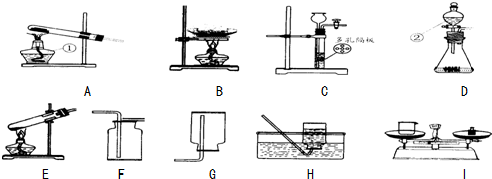
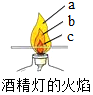 如图把一根火柴梗横放在酒精灯的火焰中,1-2秒后取出,观察到火柴梗在a处(填a、b、c)的部分最先碳化(变黑),说明外焰温度最高.
如图把一根火柴梗横放在酒精灯的火焰中,1-2秒后取出,观察到火柴梗在a处(填a、b、c)的部分最先碳化(变黑),说明外焰温度最高.