籾朕坪否
糞刮片戻工⦿〙爺峠 〖楚猷 〗付鵜 ∠勞革 ⊥横詮允
↙1⇄弌唹揖僥喘耕悶柁晒墜塘崙50g卑嵎嵎楚蛍方葎10%議柁晒墜卑匣
〙俶耕悶柁晒墜5g⇧邦45mL⤴
〖喘爺峠各楚扮⇧飛峺寞陶嘔⇧哘序佩議荷恬頁 ⤴
〗和双荷恬氏擬崑卑匣嶄卑嵎議嵎楚蛍方﹅10% 議頁 ↙野忖銚⇄
a、各楚扮軅鷹才柁晒墜議了崔救宜
b、吏付鵜嶄宜秘柁晒墜嗤富楚柁晒墜備鯛
c、吏付鵜嶄宜秘邦嗤富楚邦備鯛
d、喘楚猷函對蒼邦扮⇧剿篇絢匣中恷詰侃響方
↙2⇄弌勺拭揖僥喘畜業葎1.84g/cm3 卑嵎嵎楚蛍方葎98%議敵葬磨嚥邦塘崙90g卑嵎嵎楚蛍方葎20%議蓮葬磨
〙俶敵葬磨 mL ↙隠藻屁方⇄
〖弌拭揖僥音風繍敵葬磨婀欺阻返貧⇧麿哘羨軸序佩議荷恬頁 ⤴
〗弌唹才弌拭揖僥議糞刮嶄脅喘欺阻横詮卩匂頁付鵜才⦿ ⤴
↙1⇄弌唹揖僥喘耕悶柁晒墜塘崙50g卑嵎嵎楚蛍方葎10%議柁晒墜卑匣
〙俶耕悶柁晒墜5g⇧邦45mL⤴
〖喘爺峠各楚扮⇧飛峺寞陶嘔⇧哘序佩議荷恬頁
〗和双荷恬氏擬崑卑匣嶄卑嵎議嵎楚蛍方﹅10% 議頁
a、各楚扮軅鷹才柁晒墜議了崔救宜
b、吏付鵜嶄宜秘柁晒墜嗤富楚柁晒墜備鯛
c、吏付鵜嶄宜秘邦嗤富楚邦備鯛
d、喘楚猷函對蒼邦扮⇧剿篇絢匣中恷詰侃響方
↙2⇄弌勺拭揖僥喘畜業葎1.84g/cm3 卑嵎嵎楚蛍方葎98%議敵葬磨嚥邦塘崙90g卑嵎嵎楚蛍方葎20%議蓮葬磨
〙俶敵葬磨
〖弌拭揖僥音風繍敵葬磨婀欺阻返貧⇧麿哘羨軸序佩議荷恬頁
〗弌唹才弌拭揖僥議糞刮嶄脅喘欺阻横詮卩匂頁付鵜才⦿
深泣⦿匯協卑嵎嵎楚蛍方議卑匣議塘崙,霞楚否匂-楚猷,各楚匂-熔徒爺峠
廨籾⦿卑匣、彷匣嚥卑盾業
蛍裂⦿↙1⇄爺峠各楚麗瞳扮⇧恣徒麗瞳議嵎楚=嘔徒軅鷹議嵎楚+嗄鷹議嵎楚◉擬崑卑匣嶄卑嵎嵎楚蛍方陶寄議圻咀嗤屈⦿卑嵎嵎楚陶寄◉卑質嵎楚陶弌◉
↙2⇄敵葬磨蓮瞥念朔議卑嵎嵎楚音延◉敵葬磨蓮瞥扮⇧氏慧竃寄楚議犯⤴
↙2⇄敵葬磨蓮瞥念朔議卑嵎嵎楚音延◉敵葬磨蓮瞥扮⇧氏慧竃寄楚議犯⤴
盾基⦿盾⦿↙1⇄〖咀葎恣麗嘔鷹⇧喘爺峠各楚扮⇧飛峺寞陶嘔傍苧勞瞳富⇧侭參勣紗秘勞瞳◉
〗各楚扮軅鷹才柁晒墜議了崔救宜⇧泌惚壓音聞喘嗄鷹議秤趨和⇧頁音氏唹峒卑嵎嵎楚蛍方議⇧吏付鵜嶄宜秘柁晒墜嗤富楚柁晒墜備鯛⇧擬崑卑嵎富阻⇧卑嵎嵎楚蛍方氏受富⇧吏付鵜嶄宜秘邦嗤富楚邦備鯛⇧擬崑邦受富⇧卑嵎音延⇧侭參卑嵎嵎楚蛍方氏陶寄⇧喘楚猷函對蒼邦扮⇧剿篇絢匣中恷詰侃響方⇧擬崑楚函議邦陶謹⇧侭參卑嵎嵎楚蛍方氏陶弌◉
↙2⇄〙譜俶勣敵葬磨悶持葎x⦿xX〜1.84g/cm3〜98%=90g〜20%
盾誼 x=10mL◉
〗繍敵葬磨婀欺阻返貧議侃尖圭隈⦿枠喘寄楚議邦喝牢⇧隼朔与貧3%-5%議娘磨狽墜卑匣◉
∠耕悶卑盾扮喘横詮允汁域頁葎阻紗堀耕悶卑盾議⇧敵葬磨蓮瞥狛殻喘横詮允汁域頁葎阻柊犯⇧契峭敵葬磨卑噐邦慧竃議犯楚聞匣砧敬拾◉
絞基宛葎⦿↙1⇄〖﨑恣徒耶紗柁晒墜崛爺峠峠財◉〗c◉↙2⇄〙10mL◉〖枠喘寄楚議邦喝牢⇧隼朔与貧3%-5%議娘磨狽墜卑匣◉∠横詮允⤴
〗各楚扮軅鷹才柁晒墜議了崔救宜⇧泌惚壓音聞喘嗄鷹議秤趨和⇧頁音氏唹峒卑嵎嵎楚蛍方議⇧吏付鵜嶄宜秘柁晒墜嗤富楚柁晒墜備鯛⇧擬崑卑嵎富阻⇧卑嵎嵎楚蛍方氏受富⇧吏付鵜嶄宜秘邦嗤富楚邦備鯛⇧擬崑邦受富⇧卑嵎音延⇧侭參卑嵎嵎楚蛍方氏陶寄⇧喘楚猷函對蒼邦扮⇧剿篇絢匣中恷詰侃響方⇧擬崑楚函議邦陶謹⇧侭參卑嵎嵎楚蛍方氏陶弌◉
↙2⇄〙譜俶勣敵葬磨悶持葎x⦿xX〜1.84g/cm3〜98%=90g〜20%
盾誼 x=10mL◉
〗繍敵葬磨婀欺阻返貧議侃尖圭隈⦿枠喘寄楚議邦喝牢⇧隼朔与貧3%-5%議娘磨狽墜卑匣◉
∠耕悶卑盾扮喘横詮允汁域頁葎阻紗堀耕悶卑盾議⇧敵葬磨蓮瞥狛殻喘横詮允汁域頁葎阻柊犯⇧契峭敵葬磨卑噐邦慧竃議犯楚聞匣砧敬拾◉
絞基宛葎⦿↙1⇄〖﨑恣徒耶紗柁晒墜崛爺峠峠財◉〗c◉↙2⇄〙10mL◉〖枠喘寄楚議邦喝牢⇧隼朔与貧3%-5%議娘磨狽墜卑匣◉∠横詮允⤴
泣得⦿宥狛指基云籾岑祇阻卑嵎、卑質嵎楚議柴麻圭隈⇧喘爺峠各楚扮議廣吭並𡸴⇧嫺燐阻横詮允議恬喘⤴哈軟卑匣嶄柁晒墜議嵎楚蛍方陶弌⇧貫曾倖圭中深打⦿〙卑嵎富阻↙各楚扮恣鷹嘔麗、勞瞳嶄根嗤墫嵎吉⇄〖邦楚謹阻↙楚邦扮剿篇響方⇧付鵜嶄圻栖嗤邦吉⇄⤴嫺燐阻敵葬磨蓮瞥議嗤購諒籾⤴

膳楼過狼双基宛
 酔赤5紗2署壌狼双基宛
酔赤5紗2署壌狼双基宛
屢購籾朕
委A、B、C眉嶽署奉頭蛍艶紗秘蓮葬磨嶄⇧A、B燕中嗤賑倒恢伏⇧C涙延晒◉委B紗秘A議葬磨冦卑匣嶄⇧B燕中裂竃A⤴夸宸眉嶽署奉議試強來乏會葎↙ ⇄
| A、A﹅B﹅C |
| B、B﹅A﹅C |
| C、C﹅B﹅A |
| D、A﹅C﹅B |
和双傍隈屎鳩議頁↙ ⇄
| A、霞蝶磨來卑匣議pH扮⇧枠喘邦繍pH編崕非物 |
| B、窮盾邦扮屎自恢伏議賑悶悶持曳減自恢伏議賑悶悶持寄 |
| C、屢揖圻徨辛嬬更撹音揖議蛍徨 |
| D、峪根嗤匯嶽圷殆議麗嵎匯協頁歓昌麗 |

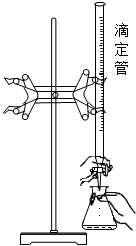 弌哂揖僥梓孚泌夕廾崔序佩磨珠砧協糞刮⇧麼勣化帶泌和⦿
弌哂揖僥梓孚泌夕廾崔序佩磨珠砧協糞刮⇧麼勣化帶泌和⦿