题目内容
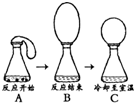 小宇同学做了一个趣味实验,她把气球中的镁屑加入到盛有稀盐酸的锥形瓶中.整个实验过程如图所示(实验装置的气密性良好),请回答下列问题:
小宇同学做了一个趣味实验,她把气球中的镁屑加入到盛有稀盐酸的锥形瓶中.整个实验过程如图所示(实验装置的气密性良好),请回答下列问题:A→B的过程中观察到气球变大,因为发生的化学反应为(用方程式表示)
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据镁和盐酸反应的现象分析;从反应生成气体,气体受热膨胀,气压增大进行分析;
解答:解:
因为镁和稀盐酸反应生成氢气,会看到溶液中产生大量的气泡;在B中因为Mg+2HCl=MgCl2+H2↑,使锥形瓶内气体增多,且反应放热使气体受热膨胀.使瓶内气压增大,大于外界大气压,在压强的作用下,气球变大.
故答案为:
Mg+2HCl=MgCl2+H2↑,增大,大于,压强.
因为镁和稀盐酸反应生成氢气,会看到溶液中产生大量的气泡;在B中因为Mg+2HCl=MgCl2+H2↑,使锥形瓶内气体增多,且反应放热使气体受热膨胀.使瓶内气压增大,大于外界大气压,在压强的作用下,气球变大.
故答案为:
Mg+2HCl=MgCl2+H2↑,增大,大于,压强.
点评:现象反映本质,抓住本实验的主要现象:气球体积的变化,对此现象进行分析,可解答对此实验所做出的一些判断.

练习册系列答案
相关题目
把铁粉和氧化铜的混合物加入到一定量的盐酸中,充分反应后,过滤.在滤液中加入少量铁粉,无现象.则下列判断正确的是( )
| A、滤渣中一定含铜 |
| B、滤液中可能含有FeCl2和HCl |
| C、滤渣可能是铜和铁的混合物 |
| D、滤液中一定含FeCl2和CuCl2 |
下图所示的实验操作中正确的是( )
A、 |
B、 |
C、 |
D、 |
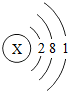 则x的值为
则x的值为