题目内容
稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法正确的是

A. 铈属于非金属元素 B. 铈的原子序数是58
C. 铈原子相对原子质量是58 D. 铈的相对原子质量是140.1g
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气(提示:CaH2+2H2O=Ca(OH)2+2H2↑).探究小组的同学把一定量的CaH2加入足量水中,充分反应后,向其中加入Na2CO3溶液,反应后过滤,得到滤渣和滤液.准确称量滤渣的质量,并检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
经过讨论,大家一致认为其中一个猜想不合理,你认为是猜想四不合理.
【实验验证】
【定量探究】过滤所得滤渣的质量为10g,求反应所得滤液中的溶质质量.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
| 猜想一:NaOH | 猜想二:NaOH、Ca(OH)2 |
| 猜想三:NaOH、Na2CO3 | 猜想四:NaOH、Na2CO3、Ca(OH)2 |
【实验验证】
| 操作 | 现象 | 结论 |
| ①取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| ②另取少量滤液,向其中滴入足量稀盐酸 | 无明显现象 | 猜想一成立 |
12.某混合气体可能含有H2、CO、CO2、HCl中的一种或几种,某同学采取实验进行检验,将混合气体先通入氢氧化钠溶液时无明显现象产生,导出的气体通过浓硫酸后再通入放有炽热氧化铜粉末的试管,发现试管中有红色物质出现.最后将试管中导出的气体依次通入放有白色硫酸铜粉末的U形管和澄清石灰水,结果白色硫酸铜粉末变蓝,澄清石灰水变浑浊.根据上述实验,可以判断混合气体中一定含有的(实验中所用试剂都过量)( )
| A. | H2 | B. | H2和CO2 | C. | CO | D. | H2、CO2和HCl |
医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
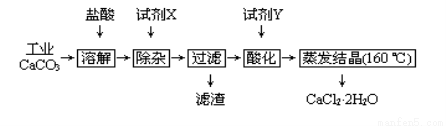
已知:查阅资料得知氢氧化物沉淀时的pH为:
氢氧化物 | Fe(OH)3 | Al(OH)3 | |
开始沉淀时的pH | 2.3 | 4.0 | 开始溶【解析】 |
完全沉淀时的pH | 3.7 | 5.2 | 完全溶【解析】 |
(1)CaCO3与盐酸反应的化学方程式_________。
(2)除杂操作是加入试剂X,调节溶液的pH范围应为________(提示:找出pH范围的两个边界值,并选择适当的数学符号“<、>、≤、≥”,组成形如 “边界值1<pH<边界值2” 等等的不等式来表示pH范围),其目的是________。试剂X最好选用________(选填序号)
a.Ca(OH)2 b.NaOH c.NH3 d.Na2CO3
(3)过滤时需用的玻璃仪器烧杯、________、_______。
(4)酸化的目的是:________。所加试剂Y名称为_______。
(5)蒸发结晶时要保持在160℃,为什么温度不能太高: _________。
(6)若所得样品CaCl2·2H2O的氯元素质量分数偏高(忽略其他实验误差),其可能原因之一是_______。
18.“绿色化学”是21世纪化学发展的主导方面.“绿色化学”要求从根本上消除污染,包括“绿色生产”和“绿色销毁”等内容.以下做法属于“绿色化学”的是( )
| A. | 将垃圾废物浇上汽油焚烧 | B. | 开发风能、太阳能等新能源 | ||
| C. | 让工业废水直接排入江河中 | D. | 用地沟油烧菜,减少浪费 |



 B.
B. 
 D.
D. 