题目内容
16.房屋在新装修后,室内空气通常含有较多甲醛,住户要注意通风,以防中毒.下列关于甲醛(HCHO)的说法,正确的是( )| A. | 甲醛是一种酸 | |
| B. | 甲醛是由氢元素、氧元素和碳元素组成的一种氧化物 | |
| C. | 甲醛有挥发性 | |
| D. | 甲醛分子中碳、氢、氧各原子的个数比为1:1:2 |
分析 A.根据酸的概念来分析;
B.根据氧化物的概念来分析;
C.根据题干信息来分析;
D.根据甲醛的分子结构来分析.
解答 解:A.电离时,产生的阳离子全部是氢离子的化合物属于酸,甲醛不属于酸,故错误;
B.氧化物的是由两种元素组成的,而甲醛中含有碳、氢、氧三种元素组成的,故错误;
C.由题干信息可知,甲醛具有挥发性,故正确;
D.由甲醛的化学式可知,甲醛分子中,碳、氢、氧各原子的个数比为1:2:1,故错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
6.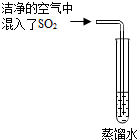 雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:
(1)要测定某地采集到的雨水是否为酸雨,在下列提供的试剂(试纸)中宜取用D.
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH试纸
(2)已知 CO2的饱和溶液常温下pH不小于 5.6.通常空气中CO2的含量大于SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.有同学想通过如图实验寻找证据,你认为下一步的实验步骤是测定溶液的酸碱度,只要出现pH值小于5.6的实验结果,就可认定SO2溶于水有形成酸雨的可能.
(3)已知SO2与 CO2有许多化学性质是相似的.亚硫酸钙(CaSO3)是白色、难溶于水但可溶于酸的固体.某同学向一酸雨样品中滴加 CaCl2溶液(如图),观察到没有浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生.则在以上过程中不可能发生的化学反应是A
A SO2+CaCl2+H2O═CaSO3↓十2HCl.
B.SO2+2NaOH═Na2SO3+H2O
C. Na2SO3+CaCl2=CaSO3↓+2NaCl
D.H2SO3+2NaOH=Na2SO3+2H2O
E.SO2+H2O═H2SO3.
 雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:| 实验序号 | X的用量/g | Y的用量/g | 生成X2Y的质量/g |
| 1 | 6.4 | 1.8 | 7.2 |
| 2 | 9 | 3.6 | 12.0 |
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH试纸
(2)已知 CO2的饱和溶液常温下pH不小于 5.6.通常空气中CO2的含量大于SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.有同学想通过如图实验寻找证据,你认为下一步的实验步骤是测定溶液的酸碱度,只要出现pH值小于5.6的实验结果,就可认定SO2溶于水有形成酸雨的可能.
(3)已知SO2与 CO2有许多化学性质是相似的.亚硫酸钙(CaSO3)是白色、难溶于水但可溶于酸的固体.某同学向一酸雨样品中滴加 CaCl2溶液(如图),观察到没有浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生.则在以上过程中不可能发生的化学反应是A
A SO2+CaCl2+H2O═CaSO3↓十2HCl.
B.SO2+2NaOH═Na2SO3+H2O
C. Na2SO3+CaCl2=CaSO3↓+2NaCl
D.H2SO3+2NaOH=Na2SO3+2H2O
E.SO2+H2O═H2SO3.
6.保护环境、防止污染,人人应引起重视.下列反应的生成物不会污染空气的是( )
| A. | 点燃爆竹 | B. | 燃烧煤炭 | ||
| C. | 氢气通入氧化铜后加热 | D. | 氢气在氯气中燃烧 |
 2011年3月22日是第二十三个“世界水日”,今年“世界水日”的主题是“应对水短缺”.请回答下列有关问题:
2011年3月22日是第二十三个“世界水日”,今年“世界水日”的主题是“应对水短缺”.请回答下列有关问题: