题目内容
5.将4.0g Cu-Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应.过滤、称量滤液的质量.相关实验数据如下:| 反应前物质的质量/g | 反应后物质的质量/g | |
| Cu-Zn合金 | 稀硫酸 | 固体和液体的总质量 |
| 4.0 | 10 | 13.96 |
分析 根据稀硫酸和锌反应生成硫酸锌和氢气,所以反应前后减少的质量就是氢气的质量进行解答.
解答 解:设铜锌合金中Zn质量为x,
则生成氢气的质量=10g+4.0g-13.96g=0.04g
Zn+H2SO4=Zn SO4+H2↑
65 2
x 0.04g
$\frac{65}{x}=\frac{2}{0.04g}$
x=1.3g
答:合金中Zn的质量为1.3g
点评 此题考查的是根据化学方程式的有关计算,学会运用控制变量法来正确的分析处理表中的数据是解答此题的关键.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
10.当发生紧急情况时,下列做法不合理的是( )
| A. | 厨房内天然气泄漏,立即关闭阀门、开窗通风 | |
| B. | 酒精灯被碰倒起火,立即用湿抹布盖灭 | |
| C. | 炒菜时油锅着火,立即浇水灭火 | |
| D. | 浓氢氧化钠溶液沾到手上,立即用大量清水冲洗,然后涂上硼酸溶液 |
15.下列有关分子、原子、离子的说法正确的是( )
| A. | 分子是保持物质性质的粒子 | B. | 原子得失电子后形成离子 | ||
| C. | 物质都是由分子构成的 | D. | 原子是由原子核、中子、电子构成 |
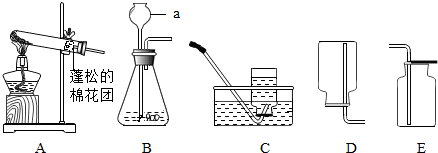
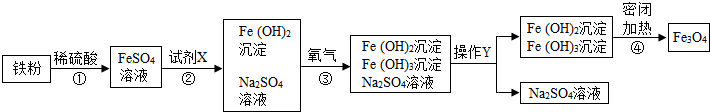 (1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是黑色.
(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是黑色.