题目内容
13.某氯化钠溶液中含有少量的氯化钡和氢氧化钠溶液杂质,它们的质量比为13:10.欲将两种杂质同时除去,得到纯净的氯化钠溶液,可选用的试剂组合是( )| A. | 盐酸和硫酸溶液,其溶质的质量比为73:49 | |
| B. | 盐酸和硫酸钠溶液,其质量比为73:71 | |
| C. | 硫酸和硫酸钠溶液,其质量比为98:71 | |
| D. | 硫酸和硫酸镁溶液,其溶质的质量比为49:60 |
分析 本题属于除杂质题,还包含了有关的计算.一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.氯化钠溶液中含有少量的氯化钡溶液杂质,可以用硫酸(或硫酸钠)除去;含有的氢氧化钠溶液杂质,可以用稀盐酸除去,还要注意滴加试剂的先后顺序.再根据有关化学方程式的计算,计算出所需要的质量比即可.
解答 解:A、设硫酸的质量为x;生成氯化氢的质量为y;氢氧化钠共需要盐酸的质量为z
BaCl2+H2SO4=BaSO4↓+2HCl NaOH+HCl=NaCl+H2O
208 98 73 40 36.5
13g x y 10g z
$\frac{208}{13g}$=$\frac{98}{x}$ $\frac{208}{13g}$=$\frac{73}{y}$ $\frac{40}{10g}$=$\frac{36.5}{z}$
x=6.125g y=4.5625g z=9.125g
z-y=9.125g-4.5625g=4.5625g
因此,盐酸和硫酸溶液的溶质的质量比为:$\frac{4.5625g}{6.125g}$=$\frac{73}{98}$ 故选项A错误;
B、设氢氧化钠需要盐酸溶质的质量为x,硫酸钠的质量为y
NaOH+HCl=NaCl+H2O BaCl2+Na2SO4=BaSO4↓+2NaCl
40 36.5 208 142
10g x 13g y
$\frac{40}{10g}$=$\frac{36.5}{x}$ $\frac{208}{13g}$=$\frac{142}{y}$
x═9.125g y═8.875g
因此,盐酸和硫酸钠溶液的溶质的质量比为:$\frac{9.125g}{8.875g}$=$\frac{73}{71}$ 故选项B正确;
C、用硫酸和硫酸钠溶液时,也会加入新的杂质硫酸钠.故选项C不正确;
D、用硫酸和硫酸镁溶液,会加入新的杂质氯化镁,故选项D不正确;
故选:B
点评 本考点属于物质的除杂或净化的探究,又结合了根据化学方程式的计算,属于难度比较大的题,也是学生经常出错的题型.综合性比较强,要牢记除杂质的条件,并认真分析,综合把握,从而突破本难点.

| 选項 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | Cu粉 | Fe粉 | 磁铁吸引 |
| C | CaO | CaCO3 | 高温 |
| D | Cu | CuO | 加入足量的稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 水是一种最常见的溶剂 | |
| B. | 地球上的水资源丰富,所以可以不用节约用水 | |
| C. | 城市生活污水、工业废水应遵循“先净化,后排放”的原则 | |
| D. | 保持水的化学性质的最小粒子是水分子 |
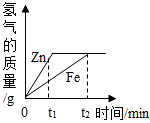 一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法正确的是( )
一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法正确的是( )| A. | t1时,产生氢气的质量锌比铁小 | B. | t1时,产生氢气的速率锌比铁大 | ||
| C. | t2时,参加反应锌的质量与铁相同 | D. | t2时,锌、铁消耗的盐酸质量相同 |
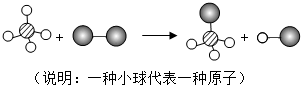 已知某两种物质在光照条件下能发生化学反应,如图所示为其微观示意,则下列说法正确的是(说明:图中原子间的短线代表原子的结合)( )
已知某两种物质在光照条件下能发生化学反应,如图所示为其微观示意,则下列说法正确的是(说明:图中原子间的短线代表原子的结合)( )| A. | 图示中的反应物都是单质 | B. | 化学反应过程中原子是可分的 | ||
| C. | 图示中共有4种分子 | D. | 该图示不符合质量守恒定律 |
| A. | 若生成物C和D分别是盐和水,则反应物可能是酸和碱 | |
| B. | 若C是单质、D为化合物,则A和B中一定一种是单质,一种是化合物 | |
| C. | 若B是酸,则C和D一定有一种是盐 | |
| D. | 若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g |
| A. | KClO3固体(KCl)--高温加热 | |
| B. | CO气体(CO2气体)--依次通入浓硫酸和足量的氢氧化钠溶液 | |
| C. | N2(O2)--反复通过灼热的铜丝网 | |
| D. | FeSO4溶液(CuSO4溶液)--滴加适量氢氧化钠溶液,过滤 |
