题目内容
15.微粒是构成化学物质的基础,下列对微粒的描述正确的是( )| A. | 原子中一定含有质子、中子、电子 | |
| B. | 氯离子的离子结构示意图为 | |
| C. | 仅由碳原子构成的物质属于纯净物 | |
| D. | NaCl是由离子构成的,所以HCl也是由离子构成的 |
分析 A、根据已有的微观构成粒子的性质和粒子之间的关系进行分析解答即可.
B、根据氯离子的结构特点分析.
C、根据碳原子构成的物质的种类分析.
D、根据构成物质的粒子分析.
解答 解:A、原子中不一定含有中子,比如氢原子,错误;
B、Cl-的离子结构示意是 ,正确;
,正确;
C、仅有碳原子构成的物质不一定属于纯净物,金刚石和石墨的混合物,仅有碳原子构成,错误;
D、HCl是由分子构成的,错误.
故选:B.
点评 本题主要考查了构成物质微粒的知识,微粒是构成化学物质的基础,应加强微粒知识的学习.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
5.下列有关实验操作的“先”与“后”的说法中,正确的是( )
| A. | 制取气体时,先装药品,后检查装置的气密性 | |
| B. | 加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 加热试管内的药品时,先预热,再加热 | |
| D. | 点燃可燃性气体时,先点燃使用,后验纯 |
10.将一定量的稀HCl加入到盛有NaOH溶液的烧杯中,未观察到明显现象.对“反应后溶液中的溶质是什么?”同学们提出了以下的猜想:
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
根据上述实验结果,同学们得出猜想二是正确.
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 | 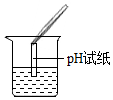 | 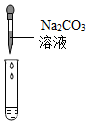 |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
20. 室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示.下列有关说法不正确的是( )
室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示.下列有关说法不正确的是( )
 室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示.下列有关说法不正确的是( )
室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示.下列有关说法不正确的是( )| A. | 该图象表示的是将盐酸滴入氢氧化钠溶液中 | |
| B. | 氢氧化钠溶液和盐酸恰好完全反应时,溶液的pH等于7 | |
| C. | 当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl | |
| D. | 滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色 |
