题目内容
6.如图是初中化学实验室常见气体的制取装置: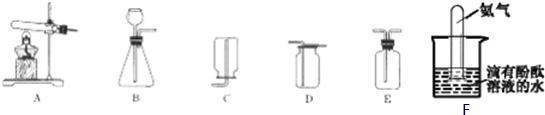
(1)实验室制取氧气的原理是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(用化学方程式表示),此原理对应的发生装置是A或B(填序号〕.用D装置收集氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(2)收集二氧化碳应选择的装置为D(填序号).理由是二氧化碳的密度比空气的密度大,欲收集一瓶干燥的二氧化碳,还需选用E装置,则E中应装入的药品是浓硫酸.
(3)加热氯化铵和熟石灰的固体混合物可制取氨气(NH3).
①制取氨气应选用的一套装置是AC(填字母代号).
②氨气极易溶于水,氨水显碱性.则图F实验可观察到什么现象?
③氨气与酸反应生成铵盐,将蘸有浓盐酸的玻璃棒靠近集满氨气的瓶口时,有大量白烟产生,而改用浓硫酸时却无此现象.请解释白烟产生的原因.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳可以用浓硫酸干燥.加热氯化铵和熟石灰的固体混合物可制取氨气(NH3),因此需要加热;氨气极易溶于水、密度比空气小,因此只能用向下排空气法收集;氨气与酸反应生成铵盐,将蘸有浓盐酸的玻璃棒靠近集满氨气的瓶口时,有大量白烟产生,是因为:浓盐酸具有挥发性,挥发出的氯化氢气体与氨气反应,生成白色的氯化铵固体的缘故.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;A或B;将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳可以用浓硫酸干燥;故答案为:D;二氧化碳的密度比空气的密度大;浓硫酸;
(3)加热氯化铵和熟石灰的固体混合物可制取氨气(NH3),因此需要加热;氨气极易溶于水、密度比空气小,因此只能用向下排空气法收集;氨气与酸反应生成铵盐,将蘸有浓盐酸的玻璃棒靠近集满氨气的瓶口时,有大量白烟产生,是因为:浓盐酸具有挥发性,挥发出的氯化氢气体与氨气反应,生成白色的氯化铵固体的缘故;故答案为:①AC;②试管内液面上升,酚酞试液由无色变红色;③浓盐酸具有挥发性,挥发出的氯化氢气体与氨气反应,生成白色的氯化铵固体的缘故;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | H+ SO42- K+ CO32- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | Fe3+ SO42- H+ Cl- | D. | Na+ Ba2+ NO3- SO42- |
| A. | 属于同一种元素 | B. | 质子数相同 | ||
| C. | 核外电子数相同 | D. | 具有相同的电子层数 |
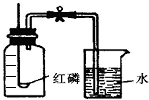 通过实验现象和题给信息,按要求填空.为测定空气的成分按如图进行实验:
通过实验现象和题给信息,按要求填空.为测定空气的成分按如图进行实验: