题目内容
7.为证明水中含有氢元素,有多种实验方法可行.①电解水的实验可证明水中含有氢元素,该反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;请再列举一种实验方法氢气在氧气中燃烧(下列②中方法除外).
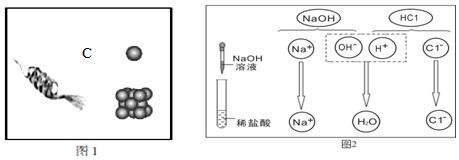
②实验室也可以利用氢气还原氧化铜的方法,装置如图1所示(图中浓硫酸起干燥作用):

“A”中盛放锌和稀硫酸的玻璃仪器名称是锥形瓶.根据无水硫酸铜由白色变蓝色现象,就可以判断有水生成,进一步得出水中有氢元素.
③“C”中如果有8g氧化铜参加反应,理论上可以得到的水有多少g?含有水分子有多少个?(请根据化学方程式列式计算)
a.水有多少g?
b.水分子有多少个?
④实验完毕,装置中药品的质量一定减轻的是AC(选填上图装置编号:A、B、C、D、E).有机物中一定含有碳元素(填写元素名称),许多有机物中也同样含有氢元素.为证明甲烷中含有氢元素,回答相关问题:
⑤如果进行如图2实验,通过燃烧证明有氢元素,该实验方法中看到的现象是烧杯内壁有水珠生成.
⑥如果进行分解实验,只要证明有氢气单质生成,也可证明甲烷中有氢元素.
分析 ①根据化学方程式的书写方法和质量守恒定律进行分析;
②根据常见仪器的名称和五水硫酸铜的性质进行分析;
③根据化学方程式分析计算即可;
④A中锌和稀硫酸反应生成氢气和硫酸锌,氢气导出,装置中药品质量减轻;B中浓硫酸吸收氢气中的水蒸气,质量增加;C中氢气还原氧化铜生成水蒸气和铜,水蒸气导出,装置中药品质量减轻;D中无水硫酸铜吸收生成的水蒸气,质量增加;E中吸收空气中的水蒸气,质量增加;有机物中一定含有碳元素.
⑤根据质量守恒定律进行分析即可;
⑥根据质量守恒定律,只要证明有氢气单质生成,也可证明甲烷中有氢元素.
解答 解:①水在通电的条件下生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢气在氧气中燃烧也能证明水是由氢元素和氧元素组成的;故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢气在氧气中燃烧;
②“A”中盛放锌和稀硫酸的玻璃仪器名称是锥形瓶.无水硫酸铜遇水变蓝,因此根据无水硫酸铜由白色变蓝色,就可以判断有水生成.故填:锥形瓶;无水硫酸铜由白色变蓝色;
③设生成水的质量为x,则
CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu
80 18
8 g x
$\frac{80}{18}$=$\frac{8g}{x}$,解得x=1.8 g
含有水分子的个数为$\frac{1.8g}{18g/mol}$×6.02×1023个/mol=6.02×1022个,答:a.水有1.8g;b.水分子有6.02×1022个.
④A中锌和稀硫酸反应生成氢气和硫酸锌,氢气导出,装置中药品质量减轻;B中浓硫酸吸收氢气中的水蒸气,质量增加;C中氢气还原氧化铜生成水蒸气和铜,水蒸气导出,装置中药品质量减轻;D中无水硫酸铜吸收生成的水蒸气,质量增加;E中吸收空气中的水蒸气,质量增加.因此实验完毕,装置中药品的质量一定减轻的是AC.有机物中一定含有碳元素.
故填:AC;碳元素;
⑤如果进行如图2实验,通过燃烧证明有氢元素,该实验方法中看到的现象是烧杯内壁有水珠生成,故填:烧杯内壁有水珠生成.
⑥如果进行分解实验,根据质量守恒定律,只要证明有氢气单质生成,也可证明甲烷中有氢元素,故填:氢气.
点评 此题难度不大,但考查知识点较多,掌握化学方程式的书写、质量守恒定律以及分析实验的能力等即可顺利解答.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 分子质量很小 | B. | 分子之间有间隔 | C. | 分子在不断运动 | D. | 分子体积很小 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 向盛有浓硫酸的烧杯中,加水进行稀释 | |
| B. | 蒸发溶液得溶质实验中,要把溶液蒸干再停止加热 | |
| C. | 测溶液PH值时,要用蒸馏水先润湿PH试纸 | |
| D. | 称量氢氧化钠质量时,要在小烧杯中快速称量 |
| A. | 氢气,水,甲烷 | B. | 盐酸,氧化镁,维生素C | ||
| C. | 不锈钢,液氧,淀粉 | D. | 石油,二氧化硫,碳酸钠 |
| A. | 用粮食发酵酿酒 | B. | 用小苏打治胃酸过多 | ||
| C. | 用石油合成塑料 | D. | 用铜制作导线 |
 如图所示(部分生成物未标出),已知在常温下,A、B、D是初中所学三种无色、无味的气体,I是一种碱,请回答下列问题:
如图所示(部分生成物未标出),已知在常温下,A、B、D是初中所学三种无色、无味的气体,I是一种碱,请回答下列问题: