题目内容
除去下列物质中混有的少量杂质(括号内为杂质),所用试剂和方法都正确的是( )
| A、Fe2O3中的(Fe):加入足量稀盐酸 |
| B、Na2CO3溶液中的(NaCl):加入稀盐酸 |
| C、FeCl2溶液中的(CuCl2):加入过量铁粉,过滤 |
| D、Ca(OH)2溶液中的(NaOH):加入过量CuCl2溶液,过滤 |
考点:物质除杂或净化的探究,金属的化学性质,碱的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、Fe和Fe2O3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、Na2CO3溶液能与稀盐酸反应生成氯化钠、水和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、过量铁粉能与CuCl2溶液反应生成氯化亚铁和铜,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、NaOH、Ca(OH)2溶液均能与CuCl2溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
B、Na2CO3溶液能与稀盐酸反应生成氯化钠、水和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、过量铁粉能与CuCl2溶液反应生成氯化亚铁和铜,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、NaOH、Ca(OH)2溶液均能与CuCl2溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列物质露置于空气中,一段时间后,质量增加的是( )
| A、大理石 | B、双氧水 |
| C、浓盐酸 | D、烧碱 |
工业生产中,可用盐酸洗去铁材表面的氧化层,但冬天因该反应变缓而影响生产,为提高酸洗液的浓度或温度以加快反应,保证生产,可在酸洗液中加入( )
| A、烧碱 | B、生石灰 |
| C、浓硫酸 | D、硝酸铵 |
不属于碳元素的同素异形体的是( )
| A、金刚石 | B、石墨 |
| C、碳60 | D、一氧化碳 |
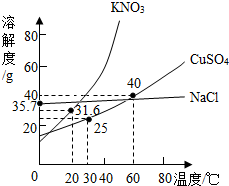 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A、40℃时将35gNaCl溶 于100g水中,降温至0℃时,可析出NaCl晶体 |
| B、20℃时KNO3饱和溶液的质量分数是31.6% |
| C、60℃时,200g水中溶解80gCuSO4达饱和,当降至30℃时,可析出30gCuSO4晶体 |
| D、30℃时,将35g KNO3和35gNaCl同时溶于100g水中,蒸发时先析出的是NaCl |
下列变化不能一步实现的是( )
| A、CO2→CO |
| B、Fe2O3→FeCl2 |
| C、Cu→Cu(NO3)2 |
| D、Na2CO3→NaOH |
 某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下: