题目内容
14.赤铁矿(主要成分为Fe2O3)是工厂里炼铁的主要原料,根据氧化铁(Fe2O3)化学式计算:(1)Fe2O3中各元素的质量比?
(2)100克含氧化铁80%的赤铁矿石中铁元素的质量?
(3)要炼得铁21吨,需含氧化铁80%的赤铁矿石多少吨?
分析 (1)根据化学式中各元素质量比等于相对原子质量与原子个数乘积之比进行计算.
(2)根据纯度的计算公式进行分析计算
(3)根据化学反应前后元素质量不变进行分析计算.
解答 解:(1)Fe203中铁元素与氧元素质量比=56×2:16×3=7:3
(2)100g含氧化铁80%的赤铁矿中氧化铁的质量=100g×80%=80g,80g氧化铁中铁元素的质量=80g×$\frac{56×2}{160}$=56g
(3)设要练得21吨铁,需含氧化铁80%的赤铁矿石的质量为x,根据化学反应前后元素质量不变可得
80%x×$\frac{56×2}{160}$=21吨
x=37.5吨
答:需含氧化铁80%的赤铁矿石37.5吨.
点评 本题主要考查根据化学式的计算,考查学生分析问题以及计算的能力.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
5.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体 | |
| B. | 置换反应生成单质和化合物,但是有单质和化合物生成的反应不一定是置换反应 | |
| C. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素、氢元素和氧元素 | |
| D. | 酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸溶液 |
2.某种氮的氧化物,氮元素和氧元素的质量比为7:20,则该化合物的化学式( )
| A. | N2O | B. | NO2 | C. | N2O5 | D. | NO |
6.下列实验操作错误的是( )
| A. |  闻气体气味 | B. | 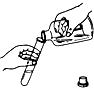 倾倒液体 | C. | 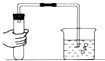 检查装置气密性 | D. | 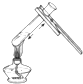 加热液体 |
4.下列对分子、原子、离子的认识,正确的是( )
| A. | 原子是最小的粒子,不可再分 | |
| B. | 温度越高,分子运动速率越快 | |
| C. | 固体难压缩,说明固体分子间无间隔 | |
| D. | 离子不能直接构成物质 |
 2010年上海世博会的场馆建设使用了大量的金属材料.
2010年上海世博会的场馆建设使用了大量的金属材料.