题目内容
9.我们日常生活中常用各种清洗剂,选择适当的用品可以得到更好的清洗效果.(1)我们使用洗洁精清洗餐具上的油污,这是因为它具有乳化功能.
(2)以下物质可以使用洁厕灵(主要成分:盐酸)清洗的是ac(填字母序号).
a.铁锈 b.油渍 c.水垢
(3)将“污渍爆炸盐”溶于水生成Na2CO3和H2O2,再加入洁厕灵,发生化学反应方程式为Na2CO3 +2HCl=2NaCl+H2O+CO2↑.
(4)化学小组发现一袋包装破损的漂白粉,同学们对漂白粉漂白作用是否失效产生疑问.(当有效成分完全消失时,则漂白粉就完全失效;部分消失时,则为部分失效).
Ⅰ.查阅资料:
①漂白粉的主要成分是Ca(ClO)2、CaCl2,其有效成分是Ca(ClO)2.
②Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO.
③HClO不稳定,易分解生成HCl和一种常见的单质气体.
④CaCl2的水溶液呈中性,HClO的水溶液呈酸性.
⑤HClO可使品红溶液褪色.
Ⅱ.交流讨论:经过分析得出:HClO分解时除生成HCl,生成的另一种常见气体是氧气
Ⅲ.实验探究:下表是探究某漂白粉是否完全失效的实验,请根据表中结论,进行填空.
| 实验步骤 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中, 通入足量CO2气体滴入适量品红溶液 | 溶液红色不褪去 | 漂白粉的漂白作用已完全失效. |
分析 (1)根据洗涤灵的去污原理分析;(2)根据洁厕灵的成分及物质的性质分析;(3)根据碳酸钠和盐酸反应的原理及化学方程式书写要求来完成;(4)交流讨论:根据质量守恒定律可知:HClO分解除生成HCl外,生成的另一种常见气体是氧气;
实验探究:根据题目信息可知,Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应Ca(ClO)2+H2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液褪色,所以就可以用品红检验
解答 解:(1)洗涤灵洗涤餐具上的油污主要是利用洗涤剂可以将油污和水溶在一起而除去,这种作用称作乳化作用;
(2)洁厕灵的成分是盐酸,可以和铁锈反应生成溶于水物质除去,可以和水垢反应生成易溶于水的物质除去,但不能和油污反应,故选ac;
(3)根据所学知识知道碳酸钠和盐酸反应生成氯化钠、水、二氧化碳气体,用观察法配平即可,二氧化碳后面标上上升符号,所以方程式是:Na2CO3 +2HCl=2NaCl+H2O+CO2↑.
(4)交流讨论:HClO不稳定,易分解生成HCl和一种常见的无色无味气体,根据质量守恒定律可知,另一种是氧气,故答案为:氧气(O2);
实验探究:根据Ca(ClO)2+H2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液褪色,所以可以利用品红颜色褪去设计实验.加入品红溶液,如果颜色不褪去,说明漂白粉失效.
故答案为:(1)乳化;(2)ac;(3)Na2CO3 +2HCl=2NaCl+H2O+CO2↑;(4)氧气;实验步骤:
| 实验步骤 | 实验现象 | 实验结论 |
| 滴入适量品红溶液 | 溶液红色不褪去 |
点评 本题主要以日常生活中常用的清洁剂为素材,考查了学生运用化学知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.现有18.6gNaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3.在室温下,将该混合物与100g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为114.2g,则原固体混合物中含有钠元素的质量为( )
| A. | 2.3g | B. | 4.6g | C. | 6.9g | D. | 9.2g |
19.柴静拍摄的纪录片《穹顶之下》播出后引发热议,唤起了公众对环保的重视,下列措施中能减少雾霾的是( )
| A. | 燃放烟花爆竹增加喜庆气氛 | B. | 鼓励开私家车出行 | ||
| C. | 推广使用太阳能热水器 | D. | 大力发展用煤火力发电 |
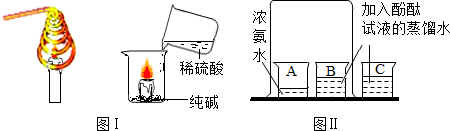
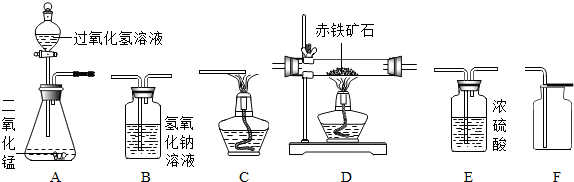
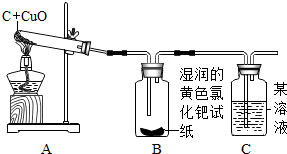
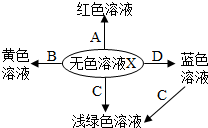 如图是化学反应的溶液颜色变化,体现了“魔法世界,魅力化学”.请据图回答:
如图是化学反应的溶液颜色变化,体现了“魔法世界,魅力化学”.请据图回答: