题目内容
一定条件下发生的某化学反应可表示为:A+3B=2C+2D(反应条件已省略).当有9.6gB完全反应时,可生成3.6gD;当反应生成4.4gC时,可生成1.8gD.那么,当有2.2gC生成时,参加反应的A的质量是 .
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律:参加化学反应的各物质的质量总和=反应后生成的各物质的质量总和.由反应A+3B=2C+2D中,由“当有9.6gB完全反应时,可生成3.6gD;当反应生成4.4gC时,可生成1.8gD”,则计算生成C物质的质量,根据质量守恒定律,可推测A的质量.判断反应中A、C物质质量关系,由反应有2.2gC生成可计算物质A的质量.
解答:解:
根据质量守恒定律,反应A+3B=2C+2D中,由“当有9.6gB完全反应时,可生成3.6gD;当反应生成4.4gC时,可生成1.8gD”,则设生成C物质的质量为x,则:
=
,解得x=8.8g;根据质量守恒定律,可推测A的质量为:8.8g+3.6g-9.6g=2.8g.根据反应中A、C物质质量关系,由反应有2.2gC生成,可设物质A的质量为y,则
=
,解得y=0.7g.
故答案为:0.7g.
根据质量守恒定律,反应A+3B=2C+2D中,由“当有9.6gB完全反应时,可生成3.6gD;当反应生成4.4gC时,可生成1.8gD”,则设生成C物质的质量为x,则:
| 3.6g |
| 1.8g |
| x |
| 4.4g |
| 2.8g |
| y |
| 8.8g |
| 2.2g |
故答案为:0.7g.
点评:本题难度不大,考查学生运用质量守恒定律进行计算的能力,由反应中各物质的质量确定反应中各物质的质量比是正确解答本题的关键.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
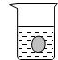 如图所示,将一个鸡蛋放入盛有稀HCl的烧杯中,我们将会观察到的现象是( )
如图所示,将一个鸡蛋放入盛有稀HCl的烧杯中,我们将会观察到的现象是( )| A、鸡蛋上有气泡产生,上浮后沉底不再上升 |
| B、鸡蛋上吸附着气泡,悬浮在溶液中 |
| C、鸡蛋上有气泡产生,上浮后下降,反复如此 |
| D、鸡蛋沉入杯底,无现象 |
下列各组实验用品,不能用于锌和铁的金属活动性强弱的是( )
| A、铁丝、硫酸锌溶液 |
| B、锌片、铁片、硫酸镁溶液 |
| C、锌片、硫酸亚铁溶液 |
| D、锌片、铁片、稀硫酸 |