题目内容
8.有甲、乙、丙三种金属,甲的盐溶液能用乙容器盛放,而不能用丙容器盛放,则三种金属的活动性顺序由弱到强的是( )| A. | 甲、乙、丙 | B. | 丙、甲、乙 | C. | 乙、甲、丙 | D. | 乙、丙、甲 |
分析 根据金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:甲的盐溶液能用乙容器盛放,说明甲的活动性小于乙,甲的盐溶液不能用丙容器盛放,说明甲的活动性大于丙,故三种金属的活动性由弱到强为乙、甲、丙,
故选C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
15.下列除杂质所选用试剂正确的是( )
| A. | 用适量稀硫酸除去NaCl溶液中的Na2CO3 | |
| B. | 用稀盐酸除去铜粉中的铁粉 | |
| C. | 用浓硫酸吸收O2中的CO2气体 | |
| D. | 用稀盐酸除去Fe2O3中的CaCO3 |
16.下列说法中,正确的是( )
| A. | 缓慢氧化与燃烧的最大区别是它不发光放热 | |
| B. | 氧气和臭氧(O3)组成元素相同,是同种物质 | |
| C. | 空气中各成分的含量是恒定不变的 | |
| D. | 液态氮比液态氧的沸点要低 |
17.取等质量的甲、乙、丙三种金属,分别投入相同浓度的盐酸中,只有乙有气泡产生;再取一小块甲投入丙的硝酸盐溶液中,甲的表面有丙析出.则甲、乙、丙三种金属的活动性顺序是( )
| A. | 乙>甲>丙 | B. | 甲>丙>乙 | C. | 丙>乙>甲 | D. | 乙>丙>甲 |
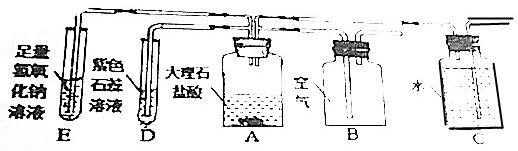
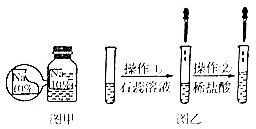 实验室有一瓶标签残缺的无色溶液(如图甲所示),其溶质是 NaCl、NaOH、和NaHCO3中的一种,为确认溶质,某同学进行了图乙的探究活动,请回答下列问题:
实验室有一瓶标签残缺的无色溶液(如图甲所示),其溶质是 NaCl、NaOH、和NaHCO3中的一种,为确认溶质,某同学进行了图乙的探究活动,请回答下列问题: