题目内容
某校化学兴趣小组将一定量的鸡蛋壳(主要成分为碳酸钙)洗净、干燥捣碎放在锥形瓶里,然后往里加入祖灵稀盐酸,实验过程和测定的相关数据如图所示.(实验中质量误差忽略不计)
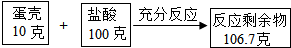
(1)共产生气体多少克?
(2)该一定量的鸡蛋壳中含碳酸钙多少克?

(1)共产生气体多少克?
(2)该一定量的鸡蛋壳中含碳酸钙多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,反应前后减少的质量是二氧化碳的质量,利用是二氧化碳的质量计算碳酸钙的质量,进而计算蛋壳中碳酸钙的质量分数.
解答:解:反应前后减少的质量是二氧化碳的质量,CO2 的质量=10g+100g-106.7g=3.3g
设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
=
x=7.5g
碳酸钙的质量分数为:
×100%=75%.
故答案为:
(1)共产生气体3.3g
(2)鸡蛋壳中碳酸钙的质量分数为75%.
设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
| 100 |
| x |
| 44 |
| 3.3g |
x=7.5g
碳酸钙的质量分数为:
| 7.5g |
| 10g |
故答案为:
(1)共产生气体3.3g
(2)鸡蛋壳中碳酸钙的质量分数为75%.
点评:利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.

练习册系列答案
相关题目
生产生活中经常用到各种消毒剂,下列对消毒剂的说法正确的是( )
| A、高锰酸钾的化学式:K2MnO4 |
| B、H2O2是由H2和O2构成的 |
| C、过氧乙酸(C2H4O3)是由碳、氢、氧三种元素组成的 |
| D、“84”消毒液中次氯酸钠(NaClO)中氯元素化合价为-1价 |

 如图是某种加钙食盐(在加碘食盐中掺适量的食用碳酸钙〕包装标签上的部分文字.为了测定此盐中的碳酸钙含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.计算此加钙食盐中碳酸钙的质量分数.
如图是某种加钙食盐(在加碘食盐中掺适量的食用碳酸钙〕包装标签上的部分文字.为了测定此盐中的碳酸钙含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.计算此加钙食盐中碳酸钙的质量分数.