题目内容
4.实验室制取气体所需的装置如下图所示,请回答下列问题:
(1)仪器a的名称是集气瓶.
(2)实验室若用A装置制氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验室若用B装置制二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)选择气体收集方法时,必须考虑的气体性质②③(填序号)①颜色 ②密度 ③溶解性 ④可燃性;收集二氧化碳所选用的装置为C(填字母);若用C装置收集氧气,验满方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)若用A、E装置来制取氧气,当导管口有气泡连续时,进行收集,集完氧气取出集气瓶后,应进行的操作是先把导气管移出水面,再熄灭酒精灯.
(5)用电解水的方法也可以制得氧气.那么若电解108g水,理论上可生成多少克氧气?
分析 集气瓶是收集气体的仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.选择气体收集方法时,必须考虑的气体性质中的密度和溶解性;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.有关化学方程式的计算要准确.
解答 解:(1)集气瓶是收集气体的仪器,故答案为:集气瓶;
(2)如果用高锰酸钾制氧气就需要加热,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑; CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)选择气体收集方法时,必须考虑的气体性质中的密度和溶解性;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:②③; C; 将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(4)实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:先把导气管移出水面,再熄灭酒精灯;
(5)解:设生成氧气的质量为x.
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
36 32
108g x
$\frac{36}{32}=\frac{108g}{x}$
x=96g
答:生成氧气的质量为96g.
故答案为:96g;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关化学方程式的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案| A. | 复合肥料:硝酸钾、过磷酸钙、磷酸二氢铵 | |
| B. | 合成材料:塑料、天然橡胶、合成纤维 | |
| C. | 有机物:甲烷、乙醇、葡萄糖 | |
| D. | 碱类:纯碱、烧碱、熟石灰 |
| A. | 豆浆 | B. | 空气 | C. | 酒精 | D. | 酱油 |
| A. | 一氧化碳通入澄清石灰水中,澄清石灰水变浑浊 | |
| B. | 打开浓盐酸的瓶塞时,瓶口冒白雾 | |
| C. | 点燃棉纱线和羊毛线,都有烧焦羽毛的气味 | |
| D. | 在空气中点燃镁条,发出耀眼的强光,生成黑色固体 |
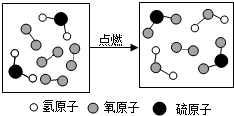
| A. | 反应物中有单质 | B. | 该反应为置换反应 | ||
| C. | 生成物的分子个数比为1:1 | D. | 化学反应前后原子的种类不变 |
| A. | 乙醚属于有机物 | B. | 乙醚由C、H、O三种原子构成 | ||
| C. | 乙醚中三种元素的质量比为4:10:1 | D. | 吸入乙醚令人神清气爽 |